Ветвями внутренней подвздошной артерии являются артерии выберите несколько вариантов
Обновлено: 08.07.2024
Аорта - самая крупная артерия нашего тела, примерно на уровне пупка, разделяется на подвздошные артерии. Подвздошные артерии проходят через малый таз в ноги и разделяются на множество артерии. У пациентов с заболеваниями артерий нижних конечностей, препятствующие кровотоку атеросклеротические бляшки обычно образуются в инфраренальном отделе аорты и подвздошных артериях. Подобные состояния называют аорто - подвздошными окклюзионными (облитерирующими) заболеваниями.
Причины аорто-подвздошных окклюзионных заболеваний
Атеросклероз является наиболее распространенной причиной формирования окклюзионных атеросклеротических бляшек в брюшном отделе аорты и подвздошных артерий. Основными факторами риска, которые приводят к возникновению атеросклеротических бляшек, в аорто-подвздошном сегменте, являются: курение, гиперхолестеринемия и сахарный диабет.
Кроме того, причиной аорто-подвздошных окклюзионных заболеваний может быть болезнь Такаясу (неспецифический артериит), который может привести к обструкции брюшной аорты и ее ветвей. Этиология болезни Такаясу до настоящего времени не известна.
Атеросклероз является чрезвычайно сложным дегенеративным заболеванием. Сегодня ученые не знают основную причину возникновения атеросклероза, однако, известны многие составляющие, которые способствуют развитию атеросклеротических поражений. Одна из наиболее популярных теорий утверждает, что атеросклероз возникает как ответ на травму артериальной стенки. Факторы, которые, как известно, способствуют травме артериальной стенки, включают в себя механические факторы, такие как гипертония и низкая эластичность стенки, а также химические факторы, таких как никотин, гиперлипидемия, гипергликемия, и гомоцистеин.
Накопление липидов начинается в гладкомышечных клетках сосудистой стенки и макрофагах в результате воспалительной реакции на травму. Отложения липидов состоят из различных композиций: холестерина, эфиров холестерина и триглицеридов. Некоторые атеросклеротические бляшки являются нестабильными, что приводит к образованию на их поверхности микротрещин. Циркулирующие тромбоциты оседают на микротрещинах и связываются с внутренними элементами бляшки. Тромбоциты связываться с фибрином посредством активации гликопротеина (GP) IIb / IIIa рецепторов тромбоцитов, и свежий кровяной сгусток формируется в области микротрещины. Подобные нестабильные атеросклеротические бляшки во многих случаях приводят к эмболии и / или распространению сгустка, который в конечном итоге может закрыть просвет артерии.
Если атеросклеротическая бляшка увеличивается в размере настолько, что перекрывает более 50% от просвета артерии, объем кровотока к нижней конечности значительно уменьшается. В состоянии покоя потребность нижних конечностей в кислороде достаточно невелика, поэтому даже при умеренных проксимальных стенозах, у пациентов может не быть никаких симптомов. В то же время во время физической нагрузки потребность тканей в кислороде возрастает и у пациентов со значимыми стенозами появляются симптомы заболевания, основным из которых является перемежающая хромота. В более запущенных случаях, происходит критическая ишемия тканей, и нейропатической боли возникают даже в состоянии покоя.
Синдром Лериша - одно из наиболее частых окклюзирующих аорто-подвздошных заболеваний артериальной системы, которое проявляется триадой симптомов:
1. Перемежающая хромота
2. Отсутствие пульсации на артериях нижних конечностей
3. Эректильная дисфункция (импотенция)
Синдром Лериша назван в честь хирурга, который впервые описал эту триаду симптомов в 1923 году. Синдром Лериша возникает при выраженном стенозе или полной окклюзии инфраренального отдела аорты обычно в результате тяжелого атеросклероза.
Синдрома Лериша может развиться в результате таких заболеваний как:
— врожденная гипоплазия или аплазия аорты;
Чаще синдром Лериша встречается при облитерирующем атеросклерозе (94%), облитерирующем эндартериите и неспецифическом аортоартериите.
Окклюзирующие поражения аорты и подвздошных артерий делят на стеноз и окклюзию. Причем могут наблюдаться не, только стеноз или окклюзия, но и их различная комбинация: стеноз брюшной аорты с односторонней окклюзией подвздошной артерии, стеноз бифуркации и обеих подвздошных артерий. Кроме того, при окклюзирующем поражении аорто-подвздошного сегмента следует оценивать состояние внутренних подвздошных, бедренных и берцовых артерий. Сочетанное поражение бедренно-подколенного сегмента встречается более чем у половины пациентов с синдромом Лериша.
Клинические проявления при синдроме Лериша зависят от степени стеноза и появляются уже при сужении артерий на 6О-7О%.
Основные симптомы синдрома Лериша
1. Боль в нижних конечностях, обусловленная хронической ишемией. При окклюзии аорты возникает, так называемая, высокая перемежающаяся хромота, которая проявляется болями в области ягодиц, пояснице и мышцах бедра. В зависимости от степени недостаточности артериального кровоснабжения условно выделяют четыре стадии ишемии (нарушения кровообращения).
Первая стадия (функциональной компенсации)
Вторая стадия (субкомпенсации)
При второй стадии перемежающаяся хромота возникает при прохождении дистанции в 200-250 метров. Кожа на стопах и голенях становится менее эластичной, сухой, шелушащейся. Нарушается рост волос на пораженной конечности, волосы выпадают, могут появиться участки облысения. В связи с нарушением кровообращения нарушается и рост ногтей, повышается ломкость, изменяется их цвет, становясь матовым, тусклым или бурым. На этой стадии начинает развиваться атрофия подкожной жировой клетчатки и мелких мышц стопы.
Третья стадия (декомпенсации)
На третьей стадии боли в конечности возникают в покое, ходьба становится возможной лишь на расстоянии 25-50 м. Характерно изменение окраски кожи в зависимости от положения пораженной конечности. Возвышенное положение конечности сопровождается ее побледнением, а опускание - покраснением кожи. При этом кожа истончается и становится легкоранимой. Незначительные травмы вследствие царапин, мозолей и ушибов приводят к образованию трещин и поверхностных язв. На этой стадии прогрессирует атрофия мышц голени и стопы.
Четвертая стадия (деструктивных изменений)
Болезненность в стопе и пальцах становятся постоянными и невыносимыми. Характерны плохо заживающие язвы, которые обычно располагаются в дистальных отделах конечностей (стопе, пальцах). Края и дно этих язв покрыты грязно-серым налетом, вокруг язв имеется воспалительная инфильтрация (покраснение). Нарастает отек стопы и голени пораженной конечности, что в конечном итоге при отсутствии медицинской помощи приводит к гангрене.
2. Вторым симптом характерным для синдрома Лериша, как уже указывалось выше, является импотенция, которая обусловлена не только ишемией тазовых органов, но и спинного мозга. Некоторые пациенты могут испытывать боль в животе сжимающего характера, возникающие при ходьбе.
3. И третий основной симптом при синдроме Лериша отсутствие пульса на бедренных артериях или его ослабление. В последнем случае врач выслушивает характерный систолический шум.

Патология подвздошных вен, которая связана с передавливанием левой подвздошной вены в малом тазу правой подвздошной артерией называют синдромом Мея Тернера. Это довольно редкое заболевание, которое поражает как мужчин, так и женщин. Синдром Мея-Тернера может являться причиной нарушения венозного оттока из левой нижней конечности и тазовых органов, вызывая варикозную трансформацию подкожных вен левой ноги, варикоцеле или варикозное расширение вен малого таза с последующим развитием хронической венозной недостаточности.
Другим компрессионным синдромом, имеющим клиническое значение при варикозе вен малого таза и семенного канатика является синдром аорто-мезентериального пинцета (nutcraker syndrome). Анатомические особенности приводят к сдавлению левой почечной вены верхней брыжеечной артерией с развитием рефлюкса по яичниковой (яичковой) вене и синдромом тазового венозного полнокровия.
Распространенность
Согласно эпидемиологическим данным правая общая подвздошная артерия (ОПА) сдавливала левую общую подвздошную вену (ОПВ) в 22 % из 430 аутопсий. В некоторых исследованиях эта находка составила до 32 %. До 16–20 % всего взрослого населения имеют бессимптомное сдавление левой ОПВ.
Течение заболевания
3 клинические стадии течения этого заболевания:
I стадия – бессимптомное течение;
II стадия – развитие сужений и штрангов в просвете подвздошной вены с явлениями хронической венозной недостаточности;
III стадия – развитие илиофеморальных тромбозов.
Прогнозы
Если стент во время операции был установлен правильно, то патология Мея Тернера не вернется. Пациенту назначают регулярное наблюдение у специалиста по сосудам и профилактическое лечение препаратами, которые предотвращают тромбоз. При естественном течении высока вероятность илеофеморального флеботромбоза слева и тяжелой хронической венозной недостаточности. Синдром аорто-мезентериального пинцета является частой причиной расстройств венозного оттока из малого таза и способствует развитию болезненных менструаций у женщин и варикоцеле у мужчин.
Преимущества лечения в клинике
Диагностика

При описании клинической картины авторы отмечают, что пациенты с синдромом Мея-Тернера предъявляют жалобы на боль и отек левой нижней конечности, боль в малом тазу, варикозное расширение вен левой нижней конечности, хронические язвы левой нижней конечности.
Женщины могут жаловаться на варикозное расширение вен половых губ, тазовые боли и/или полименорею. Чаще всего заболевание манифестирует у девочек в пубертатном возрасте, когда под действием эстрогенов происходит функциональная и морфологическая перестройка венозной системы органов малого таза.
У мужчин формируется 2-й (илеотестикулярный) тип варикоцеле, рефлюкс из подвздошной вены в яичковую. Чаще всего эти больные обращаются с жалобами на стой-кие боли в мошонке, в области таза и промежности, в левой нижней конечности, неустойчивую эрекцию, бесплодие, учащенное мочеиспускание.
Выделяют несколько групп в зависимости от клинических проявлений.
Первая группа связана с нарушением оттока из бассейна наружной подвздошной вены и вен левой нижней конечности, как следствие этого, развивается варикозная болезнь вен нижней конечности.
Вторая группа связана с нарушением оттока крови из бассейна внутренней подвздошной вены, и клинические проявления связаны с венозным полнокровием тазовых органов. Это варикозная болезнь вен малого таза у девочек и у мальчиков, сопровождающаяся синдромом тазовой боли, воспалительными заболеваниями (вульвовагинитами, простатопатиями и др.). Крайнее проявление болезни – кровотечения. До пубертатного возраста у детей чаще возникают кровотечения из прямой кишки и мочевого пузыря. Конечно, выраженность клинических проявлений зависела от степени флебогипертензии.
Обследование
УЗИ органов мошонки и подвздошных вен таза с обеих сторон. В большинстве случаев выявляется расширение левой ОПВ (общей подвздошной вены) ≥ 2 см (норма – 10–12 мм) и усиления линейной скорости кровотока в ней более чем в 2 раза по сравнению с аналогичным показателем с контрлатеральной стороны.
МР-ангиография нижней полой вены с контрастированием.
Магнито-резонансное исследование позволяет выявить варианты и степень компрессии общей, внутренней и наружной подвздошных вен слева при трехмерной реконструкции. Это исследование поможет при составлении диагностического алгоритма по пути исключения других признаков варикозной трансформации вен таза и/или нижней конечности.
Тазовая флебография
Селективные почечные и тазовые флебографии с обязательной флеботонометрией. Необходимо оценить НПВ, почечные, подвздошные и тестикулярные вены. При наличии положительного градиента давления между ОПВ слева и НПВ >10 мм рт. ст. необходимо оперативное лечение.
Клиническая больница №122 им. Л.Г. Соколова ФМБА России; Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия
Кафедра общей хирургии Санкт-Петербургской государственной медицинской академии им. И.И. Мечникова
Клиническая больница №122 им. Л.Г. Соколова ФМБА России
Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия
Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия
Хирургическое лечение больного с гигантской аневризмой внутренней подвздошной артерии
Журнал: Кардиология и сердечно-сосудистая хирургия. 2016;9(2): 71-73
Клиническая больница №122 им. Л.Г. Соколова ФМБА России; Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия





Клиническая больница №122 им. Л.Г. Соколова ФМБА России; Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия
Кафедра общей хирургии Санкт-Петербургской государственной медицинской академии им. И.И. Мечникова
Клиническая больница №122 им. Л.Г. Соколова ФМБА России
Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия
Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия
Аневризмы подвздошных артерий (АПА) чаще встречаются в ассоциации с аневризмами брюшной аорты (АБА) [1]. По данным А.А. Спиридонова [2], у 28% больных, оперированных по поводу АБА, выявляют дилатацию подвздошных артерий (ПВА). В генезе возникновения таких аневризм ведущая роль отводится атеросклерозу и связанным с ним дегенеративно-дистрофическим изменениям в сосудистой стенке. Изолированные АПА являются редким состоянием, их частота составляет 1,5-2% от числа больных с АБА [3, 7, 9]. Среди причин развития изолированных АПА указывают на травму, инфекцию, последствия беременности и родов или различные изменения в строении стенки артерии (фибромускулярная дисплазия, кистозный некроз медии и др.). Естественное течение изолированных АПА носит прогрессирующий характер и может осложниться разрывом ее стенки [5, 10]. Диагностика АПА часто бывает затруднена вследствие их асимптомного течения и локализации процесса в глубине таза. Клинические проявления возникают при достаточно больших размерах АПА и могут характеризоваться симптомами сдавления мочевого пузыря, мочеточников [4], прямой кишки [12] или периферических нервных стволов таза [8]. В 1978 г. S. Lowry и R. Kraft [6] представили на то время наиболее полный обзор литературы по данной проблеме, проанализировав 8 собственных наблюдений и 36 - из других источников. Современные методы исследования позволили значительно улучшить диагностику АПА, а разработка эндоваскулярных методов лечения способствовала расширению показаний к интервенционным вмешательствам и улучшению исходов. Свидетельством тому работа R. Uberoi и соавт. [11], где на основании анализа более 60 источников литературы обобщен современный опыт диагностики и лечения АПА. Отмечен высокий риск разрыва АПА, а значит, показания к оперативному вмешательству возникают уже при диаметре ПВА более 30-35 мм. Ведущую роль в диагностике АПА играет компьютерная томография (КТ). С учетом анатомических вариантов поражения артерий таза разработана стратегия лечения больных с АПА эндоваскулярными методами. В приведенных данных представлен опыт лечения в целом ряде клиник, причем в 6 из них число наблюдений АПА превышает 30, а в одной - свыше 50.
В настоящей работе мы представляем наблюдение изолированной аневризмы внутренней ПВА у пациента молодого возраста.
Клиническое наблюдение
Больной К., 26 лет, 27.10.14 поступил в 5-е хирур-гическое отделение Клинической больницы № 122 им. Л.Г. Соколова ФМБА РФ с диагнозом: аневризма левой внутренней ПВА. Предъявлял жалобы на расстройство мочеиспускания и эректильную дисфункцию. Из анамнеза известно, что изменения мочеиспускания возникли около 6 мес назад, в связи с чем обратился за медицинской помощью к урологу по месту жительства. В ходе обследования при проведении ультразвукового исследования (УЗИ) органов малого таза (ОМТ) было обнаружено пульсирующее образование. С целью уточнения диагноза выполнена магнитно-резонансная томография (МРТ) ОМТ: определяется округлой формы аневризматическое расширение внутренней ПВА диаметром до 10,7 см, характеризующееся гипоинтенсивным МР-сигналом во всех типах взвешенности. После внутривенного введения парамагнитного контрастирующего вещества определяется его интенсивное накопление объемным образованием с пиком в артериальную фазу сканирования. Тазовая клетчатка однородной структуры. Увеличенных лимфатических узлов и свободной жидкости в зоне сканирования не определяется. Заключение: МР-картина аневризмы левой ПВА. По результатам обследования направлен для консультации и лечения в отделение сосудистой хирургии. При изучении анамнеза данных, объясняющих возникновение аневризмы левой внутренней ПВА, не получено. Травмы, операции, инфекционные заболевания, профессиональные болезни отрицает. Наследственность не отягощена.
При объективном обследовании: больной правильного телосложения, удовлетворительного питания. При пальпации живота отмечено наличие пульсирующего образования над лонным сочленением с распространением влево, диаметром до 10 см. По данным исследования клинических и биохимических показателей крови, никаких отклонений не выявлено. Показатели системы гемостаза - в пределах нормы. Маркеры гепатита, сифилиса, ВИЧ-инфекции - отрицательные. При флюорографическом исследовании изменений со стороны органов грудной клетки не выявлено. Электрокардиограмма (ЭКГ): ритм синусовый, частота сердечных сокращений (ЧСС) 67 уд/мин. Нормальное положение электрической оси сердца, неполная блокада правой ножки пучка Гиса. Признаки гипертрофии левого желудочка (ЛЖ). При фиброгастродуоденоскопии (ФГДС): рубцовая деформация луковицы двенадцатиперстной кишки. При УЗИ органов брюшной полости - в печени, желчном пузыре, поджелудочной железе, почках патологических изменений не выявлено. На выполненной СКТ-ангиографии (рис. 1) определяется аневризма левой внутренней ПВА 100×100×100 мм с пристеночным тромбозом. Аневризматический мешок дистальнее бифуркации левой общей ПВА на 2-3 мм. Аневризма деформирует мочевой пузырь, смещая его вправо. Отмечается компрессия наружной подвздошной вены.

Рис. 1. СКТ-ангиография больного К. а - в горизонтальной плоскости; б - во фронтальной плоскости.
Наличие гигантской аневризмы левой внутренней подвздошной артерии и угроза ее разрыва явились показанием к плановому оперативному вмешательству. Учитывая размеры аневризмы и выраженную компрессию органов таза, предпочтение отдано открытому хирургическому вмешательству.
28.10.14 выполнена операция: резекция аневризмы левой внутренней ПВА.
Ход операции. Под эндотрахеальным наркозом доступом по Робу обнажено забрюшинное пространство слева. Эксплорирована левая общая ПВА в области ее деления. Левый мочеточник визуализирован. В 2 см от устья внутренней ПВА выявлена пульсирующая аневризма размером 10×10×10 см. Внутренняя ПВА пересечена проксимальнее аневризмы (рис. 2). Проксимальный конец внутренней ПВА ушит обвивным швом, дистальный - перевязан. Аневризма внутренней ПВА мобилизована, просвет ее вскрыт, тромботических масс не содержит. Отмечено массивное кровотечение из полости аневризмы, временная остановка которого была достигнута только после пережатия абдоминальной аорты. Отходящие от аневризмы ветви внутренней ПВА прошиты изнутри. Произведена резекция большей части стенки аневризмы. Гемостаз, санация раны растворами антисептиков. Забрюшинное пространство дренировано. Рана послойно ушита наглухо. Общий объем кровопотери составил 2000 мл. Для дальнейшего наблюдения транспортирован в палату интенсивной терапии.

Рис. 2. Интраоперационная фотография аневризмы левой внутренней подвздошной артерии.
Послеоперационный период протекал без осложнений, на следующие сутки переведен в хирургическое отделение. Раны зажили первичным натяжением. Через 6 дней в удовлетворительном состоянии выписан на амбулаторное лечение. При контрольном осмотре через 9 мес после операции чувствует себя хорошо, жалоб не предъявляет.
Произведено гистологическое исследование стенки аневризмы. Гистологические срезы изготавливали на микротоме Thermo Scientific HM 325, толщина срезов составила 3 мкм, использовали гистологические окраски гематоксилином и эозином по стандартной методике, пикрофуксином по методу Ван-Гизона для выявления соединительной ткани, резорцин-фуксином по Вейгерту для выявления эластических волокон. Световую микроскопию проводили на микроскопе Micros MC 20 с увеличением ×100 и ×200. Оценивали состояние соединительнотканного компонента артериальной стенки. На серии снимков представлен фрагмент артерии эластического типа. Соотношение слоев в ней сохранено, отмечается отек стенки, небольшая гипертрофия гладкомышечных клеток t. media, в t. adventitia - рассеянная лимфоцитарная инфильтрация (рис. 3). Соединительнотканные структуры t. media разной толщины, расположены беспорядочно, извиты, фрагментированы (рис. 4, 5). Эластические волокна внутренней эластической мембраны, а также t. media на большем протяжении отсутствуют, сохранившиеся - фрагментированы, извиты (рис. 6). Указанные изменения отмечены стрелками на рисунках. Заключение: гистологическая картина соответствует соединительнотканной дисплазии с нарушенным синтезом эластических и коллагеновых волокон.

Рис. 3. Артерия эластического типа. а - t. intima, б - t. media, в - t. adventitia. Окраска гематоксилином и эозином, ×100. Cтрелки указывают на отек стенки, небольшую гипертрофию гладкомышечных клеток t. media.

Рис. 4. Артерия эластического типа. Окраска гематоксилином и эозином, ×200. Cтрелки указывают на беспорядочное расположение извитых и фрагментированных соединительнотканных структур t. media.

Рис. 5. Артерия эластического типа. Окраска пикрофуксином по Ван-Гизону, ×200. Cтрелки указывают на беспорядочное расположение извитых и фрагментированных соединительнотканных структур t. media.

Рис. 6. Артерия эластического типа. Окраска резорцин-фуксином по Вейгерту, ×200.
Представленное наблюдение интересно по ряду обстоятельств, прежде всего это редкая локализация аневризмы и ее гигантские (свыше 10 см) размеры. Основным клиническим проявлением аневризмы внутренней ПВА явились нарушения уродинамики вследствие компрессии мочевого пузыря. Наконец, о причине возникновения (генез) аневризмы. С учетом возраста больного, данных клинических, лабораторных, инструментальных и гистологических методов обследования можно утверждать о врожденном характере изменений в строении стенки артерии, в виде соединительнотканной дисплазии с нарушенным синтезом эластических и коллагеновых.
Облитерирующий атеросклероз артерий нижних конечностей это заболевание, характеризующееся формированием атеросклеротических бляшек в артериях нижних конечностей, сужением просвета сосудов, нарушением кровообращения и ишемии (кислородным голоданием) конечностей при нагрузке, а затем и в покое.
Причины облитерирующего атеросклероза артерий
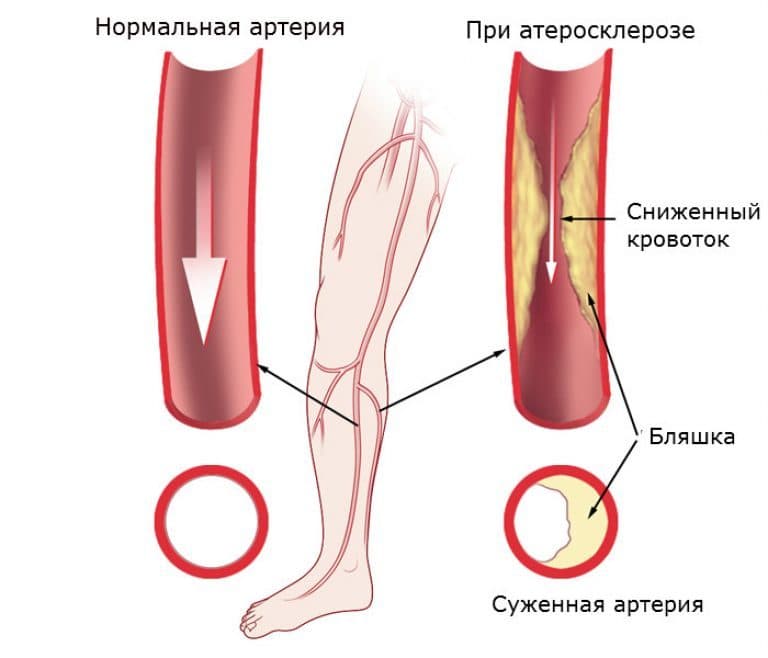
Заболевание вызывает тяжелую недостаточность кровообращения ног, обрекает больных на мучительные страдания и лишает трудоспособности. Процесс локализуется преимущественно в крупных сосудах (аорта, подвздошные артерии) или артериях среднего калибра (бедренные, подколенные артерии).
Наиболее ярким признаком ишемии нижних конечностей является перемежающая хромота, характеризующаяся появлением боли, чувством онемения и сжатия в мышцах ноги при ходьбе. Это ощущение заставляет больного остановиться, после чего боль и сжатие постепенно проходят, однако при возобновлении нагрузки боль возвращается. Пораженная нога обычно бледнее противоположной, холодная на ощупь. Даже небольшие повреждения (царапины, ушибы, потертости) заживают плохо и могут вызвать образование язв. Чувство онемения и боли в покое нередко обусловлены также ишемией нервных стволов (ишемический неврит). Длительное течение заболевания приводит к развитию гангрены и неминуемой ампутации.
Именно на дистанции ходьбы основана степень поражения сосудистого русла. Боль заставляет пациента останавливаться, дожидаясь ее исчезновения. Без лечения заболевание продолжает прогрессировать, что приводит к уменьшению дистанции ходьбы, ограничению физической активности пациента, невозможности вести привычный образ жизни. К сожалению, наиболее часто пациенты связывают данные болевые ощущения просто с мышечной усталостью, обусловленной возрастом, или с венозными проблемами, определяя боль, как судорогу, таким образом откладывая обращение за медицинской помощью и углубляя степень поражения артериального русла. В тяжелых случаях пациент не может пройти без остановки и 10 метров, но дальше становится ещё хуже: появляются боли в покое, сначала проходящие в вертикальном положении, однако через небольшой промежуток времени боли становятся постоянными, прием обезболивающих препаратов становится неэффективен. Постепенно просвет артерии сужается, приводя его к полному закрытию. Доктора вынуждены констатировать, что пациенты обращаются за мед. помощью поздно, когда поражение конечностей носит необратимый характер.
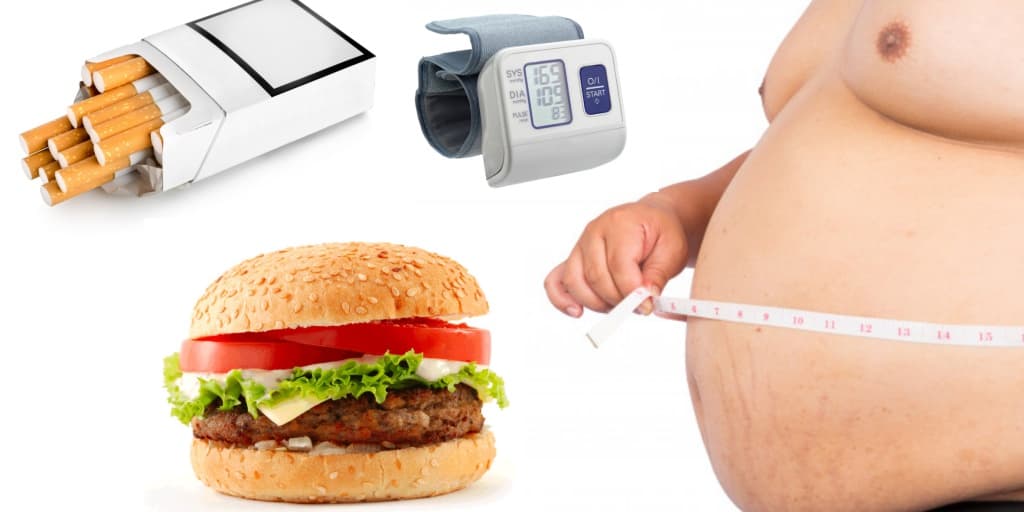
- курение;
- регулярное повышение артериального давления;
- высокая концентрация в крови общего холестерина и его составляющих;
- избыточный вес (ожирение);
- малоподвижный образ жизни (гиподинамия);
- сахарный диабет;
- сердечно-сосудистые заболевания у близких родственников.
Поражение сосудистого бассейна нижних конечностей – угрожающее жизни состояние, и в структуре смертности от сердечно-сосудистых заболеваний занимает 3-е место. Эта цифра обусловлена развитием такого тяжелого осложнения, как гангрена конечности, часто приводящая к необходимости выполнения ампутации, а при высокой ампутации летальность составляет 25%. Наряду с этим необходимо отметить и то, что 50% пациентов погибают в течение года без ампутации после постановки диагноза "критической ишемии".
Симптомы облитерирующего атеросклероза артерий нижних конечностей
Обратите внимание на следующие симптомы у себя или у своих близких:
- усталость в икроножных мышцах или мышцах бедер при прохождении 500 или менее метров,
- ощущение свинцовой тяжести в ногах или боли в мышцах, которая заставляет остановиться при ходьбе,
- изменения кожи на голенях в виде шелушения, истончения, выпадения волос.
Важно!
Это признаки атеросклеротического поражения артерий нижних конечностей. Требуется осмотр сосудистого хирурга в ближайшее время. Не удивляйтесь, если при диагностике поражений артерий нижних конечностей у Вас проверят сонные артерии и назначат кардиологическое обследование. Атеросклероз – системное заболевание, и, как правило, страдают различные группы сосудов.
При возникновении резких болей в стопе или голени одновременно с побледнением и похолоданием кожи требуется незамедлительно вызвать скорую помощь, иначе можно не успеть сохранить конечность.
Основные методы диагностики облитерирующего атеросклероза артерий нижних конечностей:
- измерение лодыжечно-плечевого индекса (лодыжечно-плечевой индекс - это параметр, позволяющий оценить адекватность артериального кровотока в нижних конечностях);
- дуплексное сканирование артерий нижних конечностей – "золотой стандарт" скринингового обследования пациентов (обнаружение и динамическое наблюдение);
- МСКТ-ангиография аорты и артерий нижних конечностей - "золотой стандарт" предоперационного обследования и в тех случаях, когда информации при УЗДС недостаточно;
- рентгенконтрастная ангиография.
Облитерирующий атеросклероз артерий нижних конечностей. Классификация заболевания (по Фонтейну-Покровскому):
- I стадия - начальные проявления стеноза - зябкость, чувство похолодания, мурашек, бледность кожных покровов, повышенная потливость, усталость в икроножных мышцах при длительной ходьбе.
- II А стадия - перемежающая хромота - скованность, чувство усталости и сжимающие боли в икроножных мышцах, возникающие при ходьбе более 200 м.
- II Б стадия - перемежающая хромота - скованность, чувство усталости и сжимающие боли в икроножных мышцах, не позволяющие пройти более 200 м.
- III стадия - выраженные боли в икроножных мышцах в покое без физической нагрузки.
- IV стадия - трофические нарушения, язвы, гангрена конечности.
Методы лечения облитерирующего атеросклероза артерий нижних конечностей:
Консервативная терапия
На ранних стадиях облитерирующего атеросклероза артерий нижних конечностей показано консервативное лечение, которое обязательно должно быть комплексным, при этом должны быть исключены все неблагоприятные факторы, вызывающие спазм сосудов. Необходимым условием успешного лечения является отказ от курения(!). Первостепенное значение придается физической активности. Больные с перемежающей хромотой должны ежедневно ходить в течение 30—45 мин — это способствует развитию мелких артерий, приводит к нарастанию мышечной силы и увеличению пройденного без боли расстояния.
При появлении боли и сжатия в мышцах ног пациент должен остановиться, а после исчезновения этих ощущений — продолжить ходьбу. Нередко езда на велосипеде или плавание переносятся значительно лучше, чем ходьба (однако не заменяют ее). Выполняется коррекция повышения артериального давления, нормализация уровня холестерина крови, уровня глюкозы крови у больных сахарным диабетом. Применяются препараты, уменьшающие тонус мелких сосудов, повышающие гибкость эритроцитов и препятствующие образованию тромбов в сосудах. Применяются также физиотерапевтические и бальнеологические процедуры, гипербарическая оксигенация.
Хирургическое лечение артеросклероза артерий нижних артерий, сосудов
Реконструктивные операции:
Рентгенэндоваскулярные методы лечения. Под контролем рентгеновских лучей при помощи специальных длинных тонких инструментов через небольшой прокол в бедренной артерии (реже - других артерий) мы можем добраться до пораженного сосуда (участка сосудов) нижних конечностей. Современные технические возможности позволяют расширить участок сосуда изнутри специальным баллоном и при необходимости установить тонкий металлический каркас (стент), препятствующий повторному сужению.
Открытые оперативные вмешательства. Больным с закупоркой сосуда по продолжительности не более 7-9 см выполняется удаление внутреннего измененного слоя артерии с атеросклеротической бляшкой и сгустками крови (эндартерэктомия). При более значительном распространении окклюзионного процесса, выраженном отложении кальция в стенке артерии показано наложение обходного пути кровотока (шунтирование) или резекция участка артерии с замещением его синтетическим протезом, либо биоматериалом (протезирование).
Если, несмотря на проводимое лечение, ишемия пораженной конечности нарастает и прогрессирует гангрена — показана ампутация: её уровень должен быть строго индивидуальным и выполняться с учетом кровоснабжения конечности.
Симптоматические вмешательства:
- Симпатэктомия (пересечение нервных сплетений, отвечающих за спазм (сужение) артерий) выполняется при повторяющихся закупорках артерий и в дополнение к реконструктивным операциям. Данная операция позволяет улучшить кровообращение в конечностях за счет расширения мелких артерий.
- Реваскуляризующая остеотомия также является вспомогательной методикой, улучшающей кровообращение за счет стимуляции образования новых мелких сосудов в нижних конечностях после повреждения кости.
- Артериализация венозного русла в данное время применяется редко, так как выполнение его сопряжено с различными техническими сложностями, а отдаленные результаты хуже вышеописанных методик.
Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
Читайте также:

