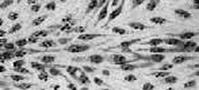
Посев вируса на культуру клеток
Добавил пользователь Skiper Обновлено: 18.09.2024
Лабораторных животных (взрослых или новорожденных белых мышей, хомяков, кроликов, обезьян и др.) заражают исследуемым вируссодержащим материалом различными способами (подкожно, внутримышечно, интраназально, интрацеребрально и др.) в зависимости от тропизма вирусов. Использование животных для культивирования вирусов в диагностических целях весьма ограничено из-за видовой невосприимчивости животных ко многим вирусам человека, контаминации животных посторонними микробами, а также по экономическим и этическим соображениям.
2. Куриные эмбрионы
Куриные эмбрионы (5-12 дневные) заражают путем введения исследуемого материала в различные полости (аллантоисная, амниотическая, желточный мешок) и ткани зародыша. Таким образом, можно культивировать вирусы гриппа, герпеса, натуральной оспы и др. Достоинствами модели являются возможность накопления вирусов в больших количествах, отсутствие скрытых вирусных инфекций, доступность для любой лаборатории.
3. Клеточные культуры
Культуру клеток (тканей) наиболее часто применяют для культивирования вирусов. Метод культур клеток разработан в 50-х годах XX века Дж. Эндерсом и соавт., получившими за это открытие Нобелевскую премию. Клетки, полученные из различных органов и тканей человека, животных, птиц и других биологических объектов, размножают вне организма на искусственных питательных средах в специальной лабораторной посуде. Большое распространение получили культуры клеток из эмбриональных и опухолевых тканей, обладающих по сравнению с нормальными клетками взрослого организма, более активной способностью к росту и размножению.
Типы тканевых культур
1. Первичные (трипсинизированные) культуры - фибробласты эмбриона курицы (ФЭК), человека (ФЭЧ), клетки почки различных животных. Их получают из клеток различных тканей путем размельчения и трипсинизации. Используют однократно, т.е. постоянно необходимо иметь соответствующие органы или ткани.
2. Линии диплоидных клеток (полуперевиваемые) пригодны к повторному диспергированию и росту, как правило, не более 40-50 пассажей (теряют исходные свойства). Их обычно получают из диплоидных клеток эмбриона человека. В процессе пассажей эти культуры сохраняют диплоидный набор хромосом, не претерпевают злокачественной трансформации, но имеют ограниченную продолжительность жизни. Так, например, пользуется известностью штамм ДКЛЧ (диплоидные клетки лёгких человека), штаммы WJT-38, JMR-90, MRC-5 из лёгких ткани эмбриона человека.
3. Перевиваемые линии (гетероплоидные культуры), адаптированы к условиям, обеспечивающим им постоянное существование in vitro, способны к многократному диспергированию и перевиванию, т.е. к многократным пассажам. Наиболее удобны в вирусологической работе - линии опухолевых клеток Hela (рак шейки матки), Hep (рак гортани).
Питательные среды, используемые для выращивания культур клеток: среда 199, среда Игла и др.
Методы индикации вирусов
Индикация вирусов – обнаружение факта их репродукции, основана на выявлении различных биологических свойств вирусов и особенностей их взаимодействия с чувствительными клетками.
Таблица 37. Методы индикации вирусов
| ЦПД (цитопатическое действие) - видимые под микроскопом морфологические изменения клеток (вплоть до их отторжения от стекла), возникающие в результате внутриклеточной репродукции вирусов. ЦПД вируса в культуре клеток можно выявить микроскопией в сроки от 3-5 суток после заражения и до 1 месяца. |
“Цветная” реакция оценивается по изменению цвета индикатора, находящегося в питательной среде культивирования. Если вирусы не размножаются в культуре клеток, то живые клетки в процессе метаболизма выделяют кислые продукты, что ведет к изменению рН среды и соответственно цвета индикатора смалинового на желтый. При репродукции вирусов нормальный метаболизм клеток нарушается (клетки гибнут), и среда сохраняет свой первоначальный малиновый цвет. III. План практической работы 1. Изучить и записать методику заражения клеточной культуры вирусом полиомиелита. Материал для исследования:смывы из зева (первые дни болезни), фекалии. Вирусологическое исследование. Выделение энтеровирусов из исследуемого материала осуществляют путем заражения клеточных культур. Для уничтожения сопутствующей бактериальной микрофлоры нестерильный материал (испражнения, глоточные смывы) предварительно обрабатывают антибиотиками (смесь пенициллина со стрептомицином, содержащая по 1000 ЕД/мл каждого антибиотика в среде 199) в течение суток при 4ºC, после чего производят контрольный посев на стерильность. При сохранении бактериальной флоры материал повторно обрабатывают теми же антибиотиками. Затем одновременно заражают по 2-3 пробирки с первичной (эмбриональные фибробласты человека или клетки почек обезьян) и перевиваемой культурой клеток (HeLa, амниона человека и др.), поскольку одни серотипы энтеровирусов лучше репродуцируются в первичных, другие – в перевиваемых клетках. Индикацию вирусов проводят по ЦПД на 2-3 день инкубации при 35 ºC. © 2014-2022 — Студопедия.Нет — Информационный студенческий ресурс. Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав (0.003) 3. Использование для вирусологического метода куриного эмбриона4. Основные способы заражения куриных эмбрионов–на хорион-аллантоисную 5. Обнаружение вирусов в курином эмбрионе• индикация: 6. Использование культур клетокКультуры клеток = соматические или 7. Первичные культуры клеток• получают из тканей (эмбриональных или 8. Перевиваемые культуры клетокПеревиваемые = стабильные = готовят из 9. Полуперевиваемые культуры клеток– диплоидные клетки различных тканей и 10. Преимущества перевиваемых культур клеток перед первичными:• продолжительность культивирования – десятки 11. Использование культур клетокЧаще – перевиваемые монослойные 12. Условия культивирования клеток:Питательные среды сложного состава (среда 199, 13. Условия культивирования клеток:Питательные среды сложного состава (среда 199, 14. Обнаружение = индикация вирусов в культуре клеток• проводят на основе следующих феноменов: 15. ЦПД = видимые под микроскопом морфологические изменения клеток (вплоть до их отторжения от стекла), возникающие в результате16. Виды ЦПД• округление и сморщивание клеток – 17. ЦПД вирусов18. Включения= скопление вирионов или отдельных их 19. Тельца Бабеша-Негри20. Бляшки, или “негативные” колонии= ограниченные участки разрушенных вирусами 21. Реакция гемагглютинации (РГА)• основана на способности некоторых 22. Реакция гемадсорбции =РГАдс = способность культур клеток, инфицированных вирусами, адсорбировать на своей поверхности23. Реакция иммунофлюоресценции (РИФ)24. Использование лабораторных животныхвзрослые или новорожденные белые мыши, 25. Способы заражения лабораторных животных26. Обнаружение вируса при заражении лабораторных животныхобнаруживают вирус по: 27. Прионы• – белковые молекулы, способные 28. ПрионыПрионный белок может существовать в двух 29. Прионыинфекционная форма (PrPs) – 35. БАКТЕРИОФАГИ36. БАКТЕРИОФАГИ39. Строение бактериофагов• икосаэдрическая головка, 41. Нуклеиновая кислота фага• Бактериофаги (фаги) содержат ДНК или 42. В состав головки входит:• полипептид, состоящий из аспарагиновой, 43. В состав сокращающегося чехла входит:44. Морфологические типы бактериофагов• I тип (нитчатые) 46. Классификация бактериофагов по спектру действия• полифаги 47. Классификация фагов в зависимости от эффекта действия на бактериальную клетку48. Классификация фагов в зависимости от эффекта действия на бактериальную клетку49. Классификация фагов в зависимости от эффекта действия на бактериальную клеткуумеренный фаг 50. Взаимодействие фагов с бактериями• может происходить: 51. Вирулентные бактериофаги• попав в бактерию, реплицируются, 52. Взаимодействие вирулентного фага с бактериальной клеткой53. Этапы взаимодействия вирулентного фага с бактериальной клеткой =продуктивный тип взаимодействия• 1. Бактериофаги с сокращающимся чехлом 54. Взаимодействие бактериофага с оболочкой клетки55. Этапы взаимодействия вирулентного фага с бактериальной клеткой =продуктивный тип взаимодействия• 4. Инъецированная внутрь клетки нуклеиновая 56. Этапы взаимодействия вирулентного фага с бактериальной клеткой =продуктивный тип взаимодействия• 5. Образовавшиеся в разных частях клетки 57. Взаимодействие умеренного фага с бактериальной клеткойадсорбция фага на специальных рецепторах КС 58. Взаимодействие умеренного фага с бактериальной клеткой• Умеренные бактериофаги 59. Взаимодействие умеренного фага с бактериальной клеткой• При интегративном типе ДНК умеренного 60. Взаимодействие умеренного фага с бактериальной клеткой• ДНК фага, встроенная в хромосому 61. Взаимодействие умеренного фага с бактериальной клеткой• При лизогении фаги не образуются в результате 62. Взаимодействие умеренного фага с бактериальной клеткой• Профаг придает бактерии новые свойства, что 63. Применение фагов• для профилактики, 64. Практическое применение бактериофагов65. Практическое применение бактериофагов66. Практическое применение бактериофаговФагодиагностика 67. Выделение бактериофагаматериал 68. Определение активности бактериофагов = фагоиндикация69. Определение активности бактериофагов = фагоиндикация71. Определение активности бактериофагов = фагоиндикация72. Титрование фага по Грациа• МПА + разведение 74. Определение активности бактериофагов = фагоиндикация–Количественные методы: 75. Титрование фага по Аппельману76. Фаготипирование бактерий78. Фаготипирование стафилококков79. Определение спектра литического действия фагаКультивирование вирусов - выращивание вирусов в искусственных условиях. Гальтье впервые осуществил в 1879 г. культивирование вируса бешенства, заразив кролика мозгом больной собаки. Способность вируса вакцины (коровьей оспы) репродуцироваться в тканевой культуре была доказана Паркером и Наем в 1925 г. В 1931 г. Вудрафф и Э. Гудпасчер показали возможность культивирование вирусов на хорион-аллантоисной оболочке эмбрионов кур (вирус оспы птиц). Методы культивирования: • На лабораторных животных • В куриных эмбрионах • В тканевых культурах Клеточная культура – система клеток, получаемая из ткани, находящаяся в виде слоя клеток, прикрепленных к стеклу, или в виде суспензии. Подразделяются на: 1) Первичные культуры – могут быть получены практически из любого органа (почки, легкие, кожа, тимус), однако даже при систематической смене питательной среды существуют лишь до первого пересева. 2) Стабильные (перевиваемые) линии – полностью адаптированные к существованию вне организма; их получают из нормальных и раковых тканей; размножаются неограниченно долгое время. Бывают 2 типов: а) Нормальные клетки. В качестве стабильной культуры используют почки барана (ПКБ) и сердце обезьяны циномольгус (СОЦ); б) Опухолевые клетки. В качестве опухолевых используют культуру клеток Hela - рак шейки матки, Hep-1 - эпидермоидный рак гортани, Дейтройт 6 - костный мозг больного раком легкого. 3) Диплоидные (эмбриональные) культуры – получаемые из эмбриональных тканей человека и животных, сохраняющие диплоидный набор хромосом до 50 пересевов. Наиболее практическое применение получили однослойные культуры первично-трипсинизированных и перевиваемых линий клеток. Приготовление первичных (трипсинизированные) культур клеток. Берется орган → разрушается межклеточная ткань и происходит разобщение клеток путём воздействия на ткань протеолитических ферментов (трипсина, панкреатина) для последующего получения монослоя клеток на стекле. В питательной среде должен присутствовать необходимый набор из неорганических ионов, аминокислот и витаминов. Различают искусственные (полусинтетические и синтетические) и естественные питательные среды. Естественные питательные среды - это биологические жидкости (сыворотка крови, эмбриональный экстракт, асцитическая жидкость, коровья амниотическая жидкость, тканевые экстракты и др.). Питательные среды из естественных компонентов применяют редко, только для выращивания вновь изолированных тканей в начале культивирования и для поддержания очень прихотливых тканей животных. Полусинтетические питательные среды представляют собой естественные среды, подверженные первичной ферментативной обработке. К таким средам относят гемогидролизаты, гидролизат лактальбумина, аминопептид и др. Лучшими средами для культивирования культуры клеток являются синтетические питательные среды: 199 (содержит 60 компонентов: 10 аминокислот, 17 витаминов, 8 минеральных солей, 10 компонентов, входящих в состав нуклеиновых кислот и др.), Игла, Хенкса, Эрла (эти среды имеют аминокислоты, витамины, глюкозу, минеральные соли). Смена питательной среды проводится через 2-3 дня. В зависимости от назначения среды подразделяются на: ростовые и поддерживающие. Ростовые применяются в первой фазе культивирования клеток, когда необходимо стимулировать клетки на максимально ускоренный рост и размножение. Они богаты питательными веществами, что способствует активному размножению клеток. Поддерживающие применяют во второй фазе культивирования клеток после заражения культуры клеток вирусами. Они поддерживают жизнеспособность клеток. О наличии вируса в зараженной культуре клеток можно судить по цитопатическому действию (ЦПД) – это патологические изменения морфологии клеток, вплоть до их гибели, возникающие в результате репродукции вирусов, и наблюдаемые под микроскопом. Проявления ЦПД: 1. Дегенерация клеток (наблюдаются округления, изменения формы, разрушения). 2. Появление включений (Липшются – вирус герпеса; Гварниери – вирус натуральной оспы) и телец Бабеша-Негри – вирус бешенства). 3. Разрушение пласта клеток (парамиксовирусы). 4. Образование гигантских многоядерных клеток - симпластов (вирус кори). Основные методы индикации вирусов в культуре тканей: а. “+” гемагглютинация. Реакция гемагглютинации – склеивание эритроцитов при добавлении вирусосодержащего материала (есть вирус – эритроциты оседают в виде “зонтика”; нет вируса – в виде “диска”). б. “+” гемадсорбция. Реакция гемадсорбции – адсорбция эритроцитов на поверхности пораженных вирусом клеток и образуют характерные скопления (вирус гриппа вызывает агглютинацию эритроцитов островкового типа). в. Реакция нейтрализации вирусов в культуре тканей. г. Цветная реакция Солка - основана на изменении цвета питательной среды. В результате жизнедеятельности клетки в питательную среду выделяются продукты клеточного метаболизма и происходит сдвиг рН в кислую сторону, о чем свидетельствует изменение цвета среды из красного в желтый. Если вирус присутствует и реплицируется в культуре, то вследствие разрушающего действия вируса клетки дегенерируются (разрушаются, т.е. их нет), и подавляется их метаболизм, т.е. цвет среды неизменяется.
Рис. 2. Заражение куриного эмбриона на ХАО через естественную воздушную камеру Заражение через искусственную воздушную камеру применяют чаще первого, так как оно обеспечивает контакт вируссодержащего материала с большей поверхностью ХАО и, следовательно, ведет к образованию большего количества вируса. Для заражения эмбриона этим методом его помещают в штатив горизонтально зародышем вверх. В скорлупе делают два отверстия: одно небольшое над центром воздушной камеры (предназначено для отсасывания из нее воздуха), а другое диаметром 0,2-0,5 см сбоку, со стороны зародыша. Сложность метода в том, что, делая второе отверстие, необходимо осторожно снять вначале кусочек скорлупы, затем скользящим движением, не повреждая ХАО, сдвинуть подскорлупную оболочку в сторону так, чтобы через образовавшийся дефект мог пройти воздух. После этого резиновой грушей через первое отверстие отсасывают воздух из естественной воздушной камеры (рис. 4, а). В результате через боковое отверстие наружный воздух устремляется внутрь, образуя искусственную воздушную камеру, дном которой является ХАО (рис. 4, б).
, Рис. 4. Заражение куриного эмбриона на ХАО через искусственную воздушную камеру (по Николау и др.)
Рис. 5. Заражение куриного эмбриона в амниотическую полость (по Николау и др.) Первый вариант. Иногда путь заражения осуществляется на горизонтально укрепленном в штативе эмбрионе, при этом зародыш находится внизу, а желток - над ним. Отверстие в скорлупе закрывают каплей расплавленного парафина. Рис. 7. Заражение куриного эмбриона в амнион открытым способом (по Николау и др.)
Рис. 8. Отсасывание аллантоисной жидкости (по Николау) Для получения стенки желточного мешка как вируссодержащего материала желток извлекают на чашку Петри, стенку его разрезают ножницами и отполаскивают от содержимого в физиологическом растворе. Тело зародыша извлекают, удерживая его за шею (рис. 10). Читайте также: |