Черная субстанция отделяет базальную часть ножек мозга от
Добавил пользователь Алексей Ф. Обновлено: 19.09.2024
Базальные ганглии обычно изоденсивные или изотенсивные по отношению к коре головного мозга. Бледный шар содержит больше миелина по сравнению со скорлупой, поэтому бледное ядро визуализируется более гипоинтенсивным на T2WI, GRE и SWI изображениях. При старении в бледном шаре откладывается кальций, что приводит к снижению сигнала, а при кальцификации более, чем на 40% сигнал теряется на всех последовательностях. При старении также в скорлупе откладывается железо, что приводит к повышению сигнала на Т2. Данное явление часто выявляется у пациентов в возрасте от 70 до 80 лет.
В нашей работе мы стремились возродить традиционное понимание психомоторных феноменов как чего-то большего, чем просто двигательные нарушения. Ведь согласно данным последних исследований, нейрональные и биохимические механизмы, лежащие в основе психомторных нарушений, затрагивают гораздо большее число систем головного мозга, чем одна лишь дофаминергическая базально-таламо-кортикальная моторная петля. Мы построили свой обзор не по традиционной схеме, отталкиваясь от нозологий, а, скорее следуя концепции RDoC, сгруппировали информацию по различным психомоторным синдромам.
В данной работе мы приводим результаты МРТ-исследований БДР, БАР и шизофрении, посвященных поиску нейробиологических коррелятов психомоторных феноменов. В начале мы фокусируемся на том, как именно дофаминергическая субкортикально-кортикальная моторная система модулируется другими нейромедиаторными системами, в частности, серотониновыми путями (субкортикально-кортикальная модуляция). Затем мы описываем, как сенсомоторная сеть (sensorimotor network, SMN) и соответствующие двигательные функции модулируются другими, немоторными, сетями, в частности, сетью пассивного режима работы мозга (default mode network, DMN). Также мы описываем, как общая активность коры влияет на локальную активность моторных отделов коры (т.е. кортико-кортикальную модуляцию).
Изменения в ядре шва модулируют активность субкортикально-кортикальных моторных путей
Одним из важных отделов ствола мозга, влияющих на дофаминергическую моторную сеть, является серотонинергическое ядро шва (raphe nucleus, RN). Так как в настоящее время опубликовано достаточно небольшое число работ, посвященных прямому влиянию ядра шва на моторную кору, в данном разделе мы также приводим данные фМРТ исследований самого ядра шва.
Han et al. в своем исследовании изучали функциональную связность в состоянии покоя (resting-state functional connectivity, rsFC (под этим термином понимают временную корреляцию изменения активности различных зон головного мозга; то есть, две зоны считаются более функционально связанными, если паттерны их возбуждения более синхронизированы, при условии, что обе эти зоны являются частями одной функциональной сети – прим. пер.)) ядра шва с остальными зонами мозга у пациентов с БАР и БДР. Оказалось, что при БАР и при БДР наблюдаются противоположные паттерны rsFC ядра шва с остальными субкортикальными регионами, в частности, с таламусом и скорлупой. Кроме того, при биполярном расстройстве rsFC гипоталамуса была повышена, а при депрессии, наоборот, снижена. Эти находки были подкреплены результатами исследования Anand et al., в котором было обнаружено значимое снижение rsFC ядра шва с префронтальной корой и средней поясной извилиной при БДР. Кроме того, показатель rsFC ядра шва с гиппокампом и миндалиной коррелировал с выраженностью депрессивных симптомов. Наконец, Wohlschlager et al. пошли дальше исследования rsFC и изучили спектральные характеристики инфрамедленных колебаний (0,01-0,1 Гц) активности ядра шва и вентральной зоны покрышки (ventral tegmental area, VTA) у пациентов с БДР, не получавших терапию. Было обнаружено, что в обеих зонах происходит существенное усиление более низкочастотной активности, что также прямо коррелировало с выраженностью депрессивной симптоматики.
Все эти данные свидетельствуют, что при депрессии имеют место определенные изменения в самом ядре шва, а также в его связях с субкортикальными моторными зонами (таламусом и базальными ганглиями) и различными немоторными зонами коры. Однако в настоящее время крайне мало исследований, посвященных возможным функциональным изменениям ядра шва и его rsFC, а также серотонинергической дисфункции, при шизофрении. Тем не менее, в указанных выше исследованиях предполагалось, что аномалии функциональных связей ядра шва (как центральной структуры серотонинергической системы) с другими субкортикальными и кортикальными регионами могут являться трансдиагностическими феноменами. Все это оставляет открытым вопрос о связи этих аномалий с моторной функцией и особенно с психомоторными симптомами.
Модуляция дофаминовых субкортикально-кортикальных моторных путей ядром шва и серотонином в здоровом мозге
Таким образом, отвечая на вопрос, поставленный в начале раздела, можно утверждать, что ядро шва и серотонин действительно модулируют дофаминовые субкортикально-кортикальные пути. Соответственно, дофаминовые пути от черной субстанции и серотониновые пути от ядра шва можно расценивать не как первично моторные пути сами по себе, а скорее как модуляторы психомоторных функций.
Модуляция дофаминовых субкортикально-кортикальных моторных путей ядром шва и серотонином при депрессии, БАР и шизофрении
Для пациентов с манией, наоборот, характерны практически диаметрально противоположные изменения. У данных пациентов наблюдалось уменьшение rsFC ядра шва с таламусом/базальными ганглиями, а также, в отличие от пациентов с депрессией, rsFC черной субстанции была сохранна. Все вместе это приводит к увеличению rsFC таламуса с SMN, усилению активности SMN и последующей психомоторной ажитации.

Рис. 1. Биохимическая и нейрональная модуляция субкортикально-кортикальных и кортико-кортикальных механизмов психомоторных феноменов. А. Модуляция дофаминергической субкортикально-кортикальной моторной цепи ядром шва и серотонином. B. Модуляция сенсомоторной сети (SMN) сетью пассивного режима работы мозга (DMN). С. Модуляция отображения общей активности в SMN. SN – черная субстанция, RN – ядро шва, Thal – таламус.
Модуляция дофаминовой субкортикально-кортикальной моторной петли ядром шва/серотонином и другими нейромедиаторными системами – дименсиональный и транснозологический подход
Еще одно доказательство дименсиональной и транснозологической природы двусторонней «от ядра шва и от черной субстанции) модуляции активности субкортикально-кортикальной моторной петли следует из результатов недавнего исследования шизофрении. Авторы изучали две группы пациентов с шизофренией – с психомоторным возбуждением и с психомоторным торможением – и сравнивали их соответственно с группами пациентов с БАР в фазе мании (и с психомоторным возбуждением) и в фазе депрессии (с сопутствующим психомоторным торможением). Оказалось, что для пациентов, страдающих шизофренией с психомоторным торможением, характерен почти тот же паттерн изменений таламо-сенсомоторной rsFC, что и для пациентов, страдающих депрессией с психомоторным торможением, то есть, снижение rsFC таламуса с SMN и сопутствующее уменьшение rsFC ядра шва и черной субстанции с базальными ганглиями и таламусом. Аналогичное совпадение наблюдалось и у пациентов, страдающих шизофренией с психомоторным возбуждением. Наблюдаемые у таких пациентов усиление rsFC таламуса c SMN и уменьшение rsFC только ядра шва с базальными ганглиями и таламусом аналогичны соответствующим изменениям у пациентов в маниакальной фазе БАР с психомоторным возбуждением.
Хрестомайтиным примером психомоторного синдрома является кататония, являющаяся по-настоящему трансдиагностическим феноменом. Кататония может встречаться при шизофрении, БАР, БДР и при других заболеваниях. Развитие кататонии является результатом дисфункции сразу нескольких нейромедиаторных систем. Действительно, кататония, в первую очередь, проявляется двигательными нарушениями, связанными с изменениями активности сенсомоторных субкортикально-кортикальных зон. Однако кататония также характеризуется аффективными нарушениями, связанными с изменениями в немоторных зонах коры (например, с нарушениями функционирования лобно-теменных связей), что подчеркивает истинно психомоторную природу этого феномена. Соответственно, наряду с гипоактивацией дофаминергических рецепторов, при кататонии наблюдаются нарушения в других нейромедиаторных системах: гипоактивация серотониновых (5-HT2A) рецепторов, дисбаланс между активностью ГАМКА (гипоактивация) и ГАМКВ (гиперактивация) рецепторов и, вероятно, также гиперактивация глутаматных NMDA-рецепторов. С одной стороны, лоразепам и золпидем (аллостерические модуляторы ГАМКА-рецепторов) усиливают возбудимость ГАМК-ергических ингибиторных сетей в моторной коре и, таким образом, способствуют облегчению симптомов кататонии. С другой стороны, баклофен и вальпроевая кислота могут усиливать активность ГАМКв- и NMDA-рецепторов и, наоборот, усилить выраженность кататонии. Тем не менее, все же существуют некоторые данные о положительном влиянии вальпроевой кислоты, топирамата и карбамазепина на аффективные кататонические симптомы (предположительно, усиливая восприимчивость ГАМК и NMDA). Наконец, клозапин (антагонист 5-HT2A-рецепторов и агонист ГАМКB-рецепторов) компенсирует серотонинергическую гипоактивацию дисбаланс активности ГАМКA-B и, таким образом, согласно некоторым исследованиям, может уменьшать выраженность кататонии.
Другим примером транснозологического психомоторного синдрома служит паркинсонизм (сочетание тремора, ригидности и брадикинезии), являющийся, главным образом, следствием болезни Паркинсона, первично нейродегенеративной по своей природе. Однако явления паркинсонизма могут быть ассоциированы и с другими заболеваниями (например, паркинсонизм может наблюдаться у больных шизофренией). Болезнь Паркинсона, в первую очередь, характеризуется дегенерацией дофаминергических клеток черной субстанции и стриатума, однако было обнаружено, что при данном заболевании также нарушается активность серотонинергической системы. Так, при болезни Паркинсона имеет место снижение количества серотониновых транспортеров в ядре шва, что прямым образом ассоциировано с тяжестью тремора. Кроме того, при болезни Паркинсона затронуты также другие нейромедиаторные системы. Известно, что модуляторы ГАМКергической системы (золпидем и клоназепам), амантадин, антихолинергические препараты и клозапин могут улучшать двигательную симптоматику болезни Паркинсона. У пациентов с шизофренией, страдающих паркинсонизмом, наблюдаются характерные изменения объема серого вещества и активности фронто-таламических/мозжечковых и кортикальных соматосенсорных сетей, не свойственные пациентам без паркинсонизма. Эти факты дают возможность предположить существование восходящей модуляции моторных отделов коры как центрального нейронального механизма возникновения паркинсонизма при шизофрении.
Наконец, психомоторные нарушения могут наблюдаться и при других заболеваниях, в частности, при аутизме. Стоит отметить, что имеются данные об ассоциированных с данным расстройством изменениях активности дофаминергической, серотонинергической (повышенный синтез серотонина), ГАМКергической и глутаматергической систем в моторной и соматосенсорной коре, а также в стриатуме. Соответственно, блокаторы дофаминовых рецепторов, ингибиторы обратного захвата серотонина, мемантин, вальпроевая кислота, арбаклофен и акампросат в некоторых исследованиях демонстрируют эффективность в уменьшении выраженности таких психомоторных симптомов аутизма, как стереотипии, импульсивность и раздражительность.
Все эти результаты ясно демонстрируют, что модуляция ядром шва и серотонином субкортикально-кортикальной моторной петли представляют собой явление, простирающееся за рамки каких-то конкретных нозологических категорий. Она соответствует скорее направленности и выраженности психомоторных нарушений, а не какому-то конкретному диагнозу, являясь, таким образом, по-настоящему дименсиональным и транснозологическим феноменом.
Модуляция моторной петли другими корковыми сетями
Кора головного мозга включает в себя различные нейронные сети: сеть пассивного режима работы мозга (DMN), сенсорные сети (зрительная, слуховая, соматосенсорная), сенсомоторная сеть (SMN), фронтопариетальная сеть, сеть салиентности, сети внимания и многие другие. Недавние исследования показали, что все эти сети функционально взаимосвязанны. К примеру, DMN и фронтопариетальная сеть противоположности по своей активности: функциональное усиление активности одной прямо приводит к угнетению активности другой и наоборот. Что особенно интересно, SMN также, по-видимому, находится в реципрокных отношениях с другими сетями, в частности, с DMN и сенсорными сетями. В исследовании Martino et al. было продемонстрировано, что увеличение нейрональной вариабельности (вариабельность амплитуды сигнала от определенной популяции нейронов; считается, что чем выше нейрональная вариабельность, тем более активна данная популяция нейронов – прим пер.) в DMN ассоциировано с уменьшением этого параметра в SMN даже у здоровых людей.
Так же, как и в случае с субкортикальной модуляцией, это реципрокное взаимодействие в крайней степени выражено у пациентов с БАР в фазе депрессии и мании. У пациентов в депрессивной фазе наблюдается аномально высокая нейрональная вариабельность в DMN, что, следуя реципрокному механизму, сопровождалось снижением нейрональной вариабельности в SMN. Изменение этих параметров коррелировало с выраженностью симптоматики: чем больше была нейрональная вариабельность в DMN по сравнению с SMN, тем более выраженными были депрессивные симптомы. Интересно, что у пациентов в маниакальной фазе, наоборот, была снижена нейрональная вариабельность в DMN и, соответственно, повышена в SMN. Это также коррелировало с маниакальной симптоматикой: чем больше была вариабельность SMN по сравнению с DMN, тем более выраженные симптомы мании наблюдались у пациента. Стоит подчеркнуть, что именно отношение вариабельностей DMN/SMN коррелировало с тяжестью симптомов, но не абсолютные значения данных показателей сами по себе.
Данные исследования наглядно демонстрируют, что нейрональная активность в моторной коре и SMN зависит не только от субкортикальных влияний ядра шва и черной субстанции, но и от активности других, немоторных сетей коры. Самым ярким доказательством этого является реципрокное взаимодействие между DMN и SMN, а также модуляция SMN сенсорными сетями. Тем не менее, механизмы, посредством которых подобная реципрокная кортико-кортикальная модуляция ассоциирована с психомоторными функциями, еще только предстоит исследовать.
Модуляция локально-региональной активности моторной коры общей корковой активностью
В данном обзоре были показаны различные нейрональные механизмы, лежащие в основе психомоторных симптомов при различных психических заболеваниях. Это является своего рода продолжением классического взгляда на психомоторные синдромы, актуальным в настоящее время, так как было продемонстрировано, что нейрональные и биохимические механизмы возникновения психомоторных нарушений не ограничиваются дофаминовой субкортикально-кортикальной моторной петлей. Мы выявили три трансдиагностических нейробиологических механизма, лежащих в основе психомоторных функций. 1) модуляция серотонином и ядром шва дофаминергической субкортикально-кортикальной моторной петли; 2) реципрокный баланс между сетью пассивного режима работы мозга, сенсомоторной и сенсорными сетями; 3) локальная синхронизация сенсомоторной сети c глобальной активностью головного мозга.
Эти механизмы в основе своей довольно похожи. Во-первых, все три механизма зависит не от каких-то абсолютных значений, а от относительных показателей, то есть, от баланса между какими-либо параметрами. Мы столкнулись с тремя видами нейронного баланса, относящимися к различным уровням проявления психомоторных функций: 1) баланс между rsFC ядра шва и черной субстанции; 2) баланс между активностью сети пассивного режима работы мозга и соматосенсорной сети; 3) баланс между глобальной активностью мозга и локальной активностью соматосенсорной сети. Кроме того, мы выявили различные виды биохимического баланса, например, между дофамином и серотонином, формирующие психомоторные функции посредством модуляции субкортикально-кортикальных и кортико-кортикальных нейронных балансов.
Во-вторых, разобранные нами данные свидетельствуют о дименсиональной и транснозологической природе психомоторных механизмов, имеющих место не только при различных заболеваниях (например, при шизофрении, БАР или депрессии), но и в норме. Соответственно, психомоторные механизмы являются иллюстрацией преимуществ применения дименсионального транснозологического синдромного подхода (как это сделано, в частности, авторами RDoc)
В-третьих, данные примеры демонстрируют континуум здоровых и патологических психомоторных состояний, в которых задействован один и тот же механизм, но проявляющийся в различной степени. В рамках данного континуума норма соответствует средним значениям, в то время как патологические состояния расположены на противоположных концах, что, таким образом, формирует кривую в форме перевернутой буквы U (см. Рис.2)



Рис.2. Перевернутые U-образные кривые континуума различных нейробиологических механизмов психомоторной активности. А. Континуум различных видов баланса между функциональной связностью ядра шва (RN) и черной субстанции (SN) с таламусом (Thal) и его связи с сенсомоторной сетью (SMN), определяющей ее активность. B. Континуум различных видов баланса между активностью SMN и сетью пассивного режима работы мозга (DMN), определяющего уровень активности SMN. C. Континуум различных видов баланса между глобальной активностью мозга (GA) и уровнем активности SMN.
В-четвертых, первернутая U-образная кривая демонстрирует, что именно средние показатели различных видов нейробиологического баланса являются наиболее оптимальными. В отличие от них, крайние формы смещения баланса являются дисфункциональными, приводящими к нарушению психомоторных функций.
В-пятых, с клинической точки зрения психомоторные нарушения могут быть охарактеризованы специфическим набором симптомов, то есть, сочетанием определенных двигательных, аффективных и когнитивных нарушений. Например, психомоторное возбуждение может сопровождаться эмоциональными нарушениями (например, повышенными аффектом) и когнитивными нарушениями (в частности, нарушениями внимания). В то же время психомоторное торможение часто сопровождается негативными эмоциями и усилением внимания на самом себе. Подобные конструкции симптомов позволяют предположить наличие связей между субкортикально-кортикальной моторной системой и немоторными, аффективными и когнитивными, нейронными системами, что подтверждается, например, существованием реципрокных взаимодействий между SMN, DMN и сенсорными сетями.
Наконец, все перечисленные механизмы имеют потенциальное диагностическое и терапевтическое значение. Они могут применяться для ранней диагностики пограничных состояний и манифеста психических заболеваний, служить потенциальными биомаркерами терапевтического ответа и быть мишенями неинвазивных методов стимуляции головного мозга (транскраниальной магнитной стимуляции и др.) Несмотря на то, что при помощи этих методов может проводиться стимуляция разных отделов мозга, все они тем или иным образом повлияют на активность субкортикально-кортикальной моторной петли и уменьшать выраженность психомоторных нарушений. Как и в случае с Римом, все дороги, в конечном счете, ведут к моторной коре.
Ультразвуковое исследования черной субстанции головного мозга является информативным как для подтверждения, так и для исключения болезни Паркинсона, специфичность метода составляет 93,7%. УЗИ является более информативным у лиц старше 60 лет, при этом оценивается гиперэхогенность черной субстанции мозга. Гиперэхогенность черной субстанции является маркером заболевания, определяющего риск развития и факт наличия болезни Паркинсона. Основные факторы риска развития болезни Паркинсона- возраст, генетическая предрасположенность, отягощенный семейный анамнез. Транскраниальное УЗИ черной субстанции может проводиться пациентам любой возрастной группы при назначении неврологом.
Обращаем Ваше внимание на то, что в соответствии с п. 10.ст.16 Федерального Закона "Об обязательном медицинском страховании" №326-ФЗ от 29.11.2010 года, при каждом обращении за медицинской помощью в ОКДЦ, вы должны предъявить свой полис ОМС в регистратуре центра.
Как узнать результаты исследований?
В приемном отделении ОКДЦ с 8.00 до 15.00 работает процедурный кабинет, где по назначению врача, на платной основе выполняются инъекции, включая:
-внутривенно-капельную инфузию,
-внутривенно-струйную инъекцию,
-внутримышечную инъекцию,
- подкожную инъекцию,
-премедикацию (обезболивание) перед проведением исследований МРТ. СКТ, коронарографии, ФГДС, ФКС и бронхоскопии.
Если Вы хотите получить эту медицинскую услугу, Вам необходимо обратиться в регистратуру ОКДЦ, имея при себе заключение Вашего лечащего врача и его рекомендации.
Запись на повторный прием проводится только через телефон Вашего лечащего врача ОКДЦ, информация об этом имеется в маршрутном листе.
черная субстанция это гетерогенная часть среднего мозга, специфическая область мозга. Кроме того, он состоит из важного элемента системы базальных ганглиев.
В частности, он представляет собой дорсальную часть мозга, которая характеризуется наличием нейронов, содержащих нейромеланин, специфический темный пигмент мозга..
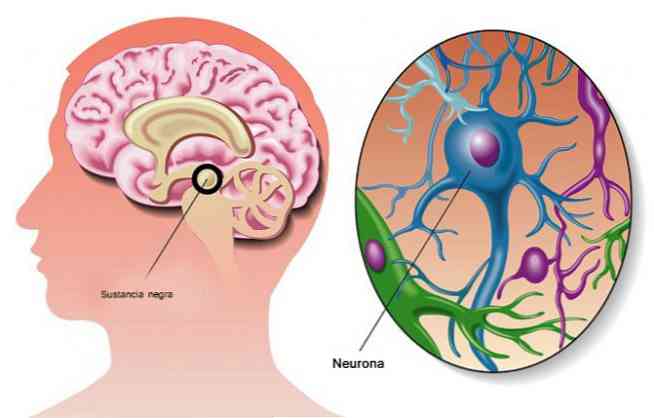
Таким образом, название черного вещества относится к самому внешнему виду, которое принимают нейроны определенных областей среднего мозга. Они имеют темный цвет, очень похожий на черный.
Черная субстанция образована дофаминергическими и ГАМКергическими нейронами и играет важную роль в контроле двигательной активности.
В этой статье мы объясняем характеристики черной субстанции, анализируем ее анатомические свойства и функции и обсуждаем заболевания, связанные с этим элементом мозга..
Анатомия черной субстанции
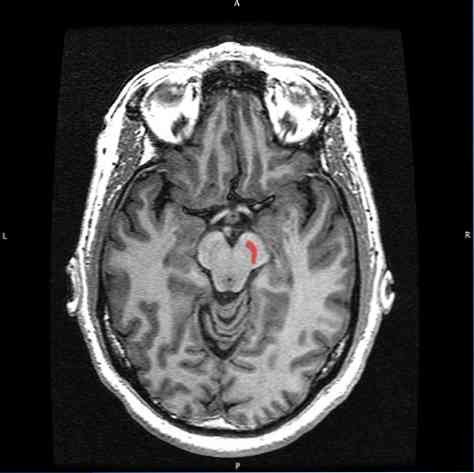
Черная субстанция представляет собой область головного мозга, которая расположена дорзально к мозговым цветоножкам и распространяется рострокаудально вдоль среднего мозга.
Первые исследования этого конкретного вещества были сделаны Мингаццини в 1888 году и Сано в 1919 году. С тех пор был сделан вывод, что черная субстанция разделена на две макроскопические части..
Первая, известная как дорсальная часть, характеризуется тем, что является веществом, очень богатым нейронами с нейромеланином. Цвет этого пигмента заставляет клетки в этой области выглядеть темнее, чем обычно.
Другая часть черной субстанции находится в более вентральной области, где расположена наиболее объемная структура черного вещества. Он имеет сплюснутую яйцевидную форму и характеризуется тем, что в клетках он беднее.
Наконец, некоторые авторы защищают существование боковой части черной субстанции. Однако в настоящее время эта часть считается частью вентральной части вещества..
С другой стороны, две части черного вещества также могут быть легко дифференцированы по типу нейротрансмиттеров, которые они включают. В то время как нейроны дорсальной части содержат высокие концентрации дофамина, нейроны вентральной части богаче ГАМК.
Нейроны черного вещества
Три основных типа нейронов были описаны в нервной системе. Они в основном различаются по размеру и местоположению.
К нейронам первого типа относятся крупные клетки, которые находятся в вентральной области черной субстанции и относятся к области, известной как ретикулярная черная субстанция..
Наконец, третий тип нейронов - это маленькие клетки, которые находятся в двух частях черного вещества, дорсальной и вентральной. То есть и черная сшитая субстанция, и компактная черная субстанция содержат маленькие нейроны.
Дофаминовые нейроны очень распространены в компактном черном веществе (дорсальная область), однако они могут располагаться в разных областях среднего мозга, включая вентральную область (черное сетчатое вещество).
Дофаминовые нейроны отличаются гистофуоресцентным и иммуногистохимическим методами, а также окрашиванием по Нисслу, так как этот тип нейронов имеет высокую массу вещества Ниссле..
Дофаминергические нейроны имеют срединное нейрональное тело, которое находится в компактном черном веществе. Представляет несколько основных дендритных процессов, обычно от 3 до 6 процессов, которые могут быть раздвоены до 4 раз.
Один или два дендрита этих нейронов вводятся в черную субстанцию ретикулярную. Аксон дофаминергических клеток происходит от одного из основных дендритов и не миелинизирован.
Аксон не испускает коллатерали внутри черной субстанции и проходит через латеральный гипоталамус до достижения полосатой области. Другие дендриты нейрона разветвляются в компактную черную субстанцию.
Черное вещество - Серое вещество - Белое вещество
Помимо черной субстанции, мозг обладает аналогичными веществами другого типа: белым веществом и серым веществом..
Принцип этих областей мозга одинаков. Они представляют собой церебральные структуры, изобилующие нейронами, и их название связано главным образом с появлением клеток такого типа..
То есть нейроны, относящиеся к черной субстанции, темные, нейроны серого вещества имеют более серый цвет, а те, что в белом веществе, характеризуются этим цветом.
Тем не менее, цвет не единственный элемент, который отличает одно вещество от другого. В этом смысле наиболее важные элементы, которые мотивируют каталогизацию каждого типа вещества, находятся в расположении, анатомии и функциях их нейронов..
Серое вещество
Серое вещество находится в коре головного мозга и в центре спинного мозга (области, где нет ни белого вещества, ни черного вещества). Он состоит в основном из нейрональной сомы и дендритов, лишенных миелина.
Он содержит мотонейроны, вегетативные протонейроны, кордональные нейроны, нейроны Гольджи I типа и спинальный ганглион. Поскольку он не содержит миелин, он не способен быстро передавать нервные импульсы, и его функции заключаются главным образом в когнитивных процессах, связанных с рассуждением.
Белое вещество
Белое вещество имеет местоположение, противоположное расположению серого вещества. В головном мозге он расположен внутри (в то время как серое вещество находится снаружи и в коре), а в спинном мозге он расположен снаружи (в то время как серое вещество находится в центре).
Белое вещество также характеризуется тем, что состоит из миелинизированных нервных волокон, которые содержат несколько аксонов (но не сомы и нейрональные тела).
Что касается его функций, белое вещество активно влияет на обучение и функционирование мозга. Распределяет потенциалы действия и выступает в роли реле и координатора связи между областями мозга..
Черное вещество
Наконец, черная субстанция находится в среднем мозге, в основном в областях, которые охватывают базальные ганглии. Он содержит аксоны, дендриты и сома нейронов, и его основные функции связаны с движением и ориентацией.
Типы черной субстанции
Черная субстанция отличается от белого вещества и серого вещества своим внешним видом, расположением, структурой и функцией. Тем не менее, внутри черного вещества вы также можете выделить две конкретные области.
Эта дифференциация в основном отвечает типам нейронов, которые включает в себя черная субстанция. В некоторых регионах преобладает определенный тип клеток, а в других подключаются разные нейроны..
Аналогично, две области черной субстанции связаны с различными функциями, а также с патологиями разных видов..
Две части черной субстанции - это компактная часть и сетчатая часть. Компактная часть включает смежные дофаминергические группы, а сетчатая часть также касается латеральной части черной субстанции.
Компактное черное вещество
Компактная часть черной субстанции характеризуется черными нейронами, окрашенными через пигмент нейромеланина. Этот пигмент увеличивается с возрастом, поэтому нейроны этой области становятся темнее с годами.
Эта часть черного вещества может быть разделена между брюшным и спинным полом. Нейроны компактной части получают тормозные сигналы от коллатеральных аксонов нейронов сетчатой части черной субстанции.
Дофаминергические клетки этой области также иннервируют другие структуры системы базальных ганглиев, такие как медиальный паллидум, сетчатая часть черной субстанции и субталамическое ядро..
Его деятельность в основном связана с учебными процессами. Однако работа этого региона сложна и мало изучена в настоящее время..
Некоторые исследования предполагают, что дегенерация пигментированных нейронов компактного черного вещества представляет собой основной признак болезни Паркинсона, поэтому предполагается, что этот регион будет вовлечен в развитие патологии..
Что касается электрофизиологических исследований, некоторые авторы указывают, что нейроны этой области характеризуются наличием потенциалов действия с трехфазным сигналом, с первой положительной фазой и со средней продолжительностью более 2,5 миллисекунд..
Сетчатое черное вещество
Сшитое черное вещество отличается от компактного черного вещества плотностью нейронов, которая значительно меньше. Фактически, получается несколько диффузная область, и дендриты нейронов предпочтительно перпендикулярны рифленым афферентам..
Он состоит из гетерогенной популяции ГАМКергических нейронов, в основном проекционных нейронов большого и среднего размера, а также небольших интернейронов звездной формы..
Низкая плотность нейронов ретикулярной черной субстанции анатомически очень похожа на плотность бледного баллона и энтопедункулярного ядра. Фактически, благодаря своей цитологии, связям, нейрохимии и физиологии, ретикулярная черная субстанция может рассматриваться как продолжение этих структур мозга..
Средние нейроны имеют нейронное тело переменной формы. Он может быть треугольным, веретенообразным, яйцевидным или многоугольным, обычно содержащий от 3 до 5 первичных дендритов, которые происходят в теле нейрона.
Основные дендриты ретикулярной черной субстанции образуются на полюсах веретенообразных нейронов, дихотомически делящихся на небольшом расстоянии от тела. Третичные дендриты обычно появляются на большом расстоянии, около терминальных дендритов.
Аксоны нейронов милленизируются и происходят из организма или первичных дендритов клетки. Большинство из них попадают в черное ретикулярное вещество или в компактное черное вещество.
Что касается его функций, то сетчатое черное вещество, по-видимому, связано с процессами ориентации и окуломинации. Кроме того, эта структура мозга была связана с болезнью Паркинсона и эпилепсией.
функции
Функции черной субстанции сегодня, безусловно, противоречивы. Деятельность этих областей мозга, или какие специфические функции они выполняют, еще не была детально изучена..
Тем не менее, полученные данные о его деятельности позволяют предположить, что черная субстанция может быть вовлечена в четыре основных процесса: обучение, моторное планирование, движение глаз и поиск вознаграждения..
обучение
Связь между обучением и черной субстанцией связана с отношениями, которые эта структура имеет с болезнью Паркинсона. В настоящее время хорошо известно, что изменения в нейронах черной субстанции являются признаком дегенеративной патологии..
В этом смысле амнестические изменения, которые многие субъекты с болезнью Паркинсона привели к началу изучения роли черной субстанции в обучении.
В частности, команда исследователей из Университета Пенсильвании показала, что стимуляция дофаминергических нейронов черной субстанции может изменить процесс обучения.
Исследование проводилось в группе субъектов, которые проходили лечение от болезни Паркинсона посредством глубокой стимуляции, что объясняется улучшением ассоциативного обучения участников..
Поиск вознаграждений
В том же предыдущем исследовании было продемонстрировано, как стимуляция дофаминергических нейронов черной субстанции вызывала у людей приятные ощущения.
По этой причине утверждается, что эта структура мозга может быть тесно связана как с поиском вознаграждения, так и с зависимостью..
Моторное планирование
Роль черной субстанции в моторном планировании является одной из наиболее хорошо изученных и документированных функций..
Многие исследования показывают, как нейроны черной субстанции играют жизненно важную роль в развитии движений тела, что широко отражается в симптомах паркинсонизма, которые вызывают его дегенерацию..
Движение глаз
Наконец, также было показано, как нейроны черной субстанции вмешиваются в процессы движения глаз. Эта функция, по-видимому, в основном выполняется сшитым черным веществом.
Читайте также:

