Бокс для посевов в микробиологии
Обновлено: 07.07.2024
В автоматах для микробиологических посевов EasySpiral компании Interscience применяются новые технологии, основанные на автоматическом спиральном методе посева культур на чашках Петри в лабораторных условиях. Автоматы для микробиологических посевов EasySpiral применяются:
Контроль качества пищевых продуктов;
Определение бактериальной кинетики;
Определение минимальной ингибирующей дозы антибиотиков;
Контроль фармацевтических и косметологических препаратов.
Автоматы для микробиологических посевов EasySpiral позволяют проводить посев и все необходимые разбавления на одной чашке Петри, что снижает количество расходных материалов до 75%, а воспроизводимость и повторяемость результатов повышаются до 99,5%. Полный цикл, включающий дезинфекцию, отбор образца и посев, проводится за 25 секунд. Посев культуры на автоматах для микробиологических посевов EasySpiral происходит по траектории Архимедовой спирали, объем пробы откалиброван и известен в каждой точке чашки Петри.
Автоматы для микробиологических посевов EasySpiral с корпусом из нержавеющей стали можно размещать как внутри, так и вне ламинарных боксов. Модульная подставка для чашек Петри подходит для использования чашек Петри с диаметром 90 мм.
Инновационная система дезинфекции гарантирует отсутствие кросс-контаминации, а бутылка на 2 л обеспечивает 600 циклов чисток, при опустошении бутылки срабатывает датчик.
Ниже приведены технические характеристики автоматов для микробиологических посевов EasySpiral.
Сегодня на рынке лабораторного оборудования предлагается множество изделий, которые производители определяют как боксы микробиологической (чаще биологической) безопасности 1 . Но как узнать, соответствует ли данное изделие своему наименованию или относится к чему-либо иному? И что такое вообще бокс микробиологической безопасности — можно ли его как-то идентифицировать?
В данном вопросе можно опираться только на нормативные документы. Так, Всемирная Организация Здравоохранения (ВОЗ) дает определение назначению боксов микробиологической безопасности 2 . Существует также ГОСТ Р ЕН 12469-2010 3 (аутентичный перевод европейского стандарта EN 12469), в котором подробно описаны требования к конструктивному исполнению боксов микробиологической безопасности I, II и III классов, к методикам их проверки, технического обслуживания, обеззараживания, условиям применения. В этом же стандарте имеются указания, что, например, при работе с контаминированным (патогенным) агентом нужно использовать только боксы микробиологической безопасности I, II и III класса. Кроме того, существуют санитарные правила, соблюдение которых является обязательным для юридических лиц независимо от организационно-правовых форм и форм собственности и индивидуальных предпринимателей, проводящих работу с ПБА, и которые также указывают на необходимость использования боксов микробиологической безопасности при проведении определенных видов работ 4 .
Гарантией же того, что предлагаемое покупателю изделие соответствует заявленному виду лабораторного оборудования, может являться Регистрационное удостоверение (прилагается к изделию). Обращаем ваше внимание на то, что в регистрационном удостоверении к боксу микробиологической безопасности II класса обязательно должно быть указано, что данное изделие предназначено для защиты оператора при работе с патогенными агентами и микроорганизмами, передающимися воздушно-капельным путем. Если в регистрационном удостоверении подобной формулировки нет, то потребитель рискует приобрести изделие, не отвечающее нормативным требованиям, не относящееся к боксам микробиологической безопасности II класса и, следовательно, не предназначенное для лабораторных исследований. Таким образом, возникает риск, что надзорные органы не дадут разрешение на эксплуатацию данного изделия, лаборатория не пройдет периодическую сертификацию (валидацию), а применение изделия, не предназначенного для работы с патогенными агентами, может быть небезопасным для оператора, продукта и окружающей среды.
456300, г. Миасс, Челябинская обл., Тургоякское ш., 2/4
2 ВОЗ: Боксы биологической безопасности предназначены для того, чтобы защитить оператора, лабораторное оборудование и рабочие материалы от воздействия инфекционных аэрозолей и брызг, которые могут возникнуть при работе с материалами, содержащими инфекционные агенты, такими как первичные культуры, инвентарь, диагностические образцы (…). Бокс биологической безопасности II класса сконструирован для защиты не только персонала, но и материалов, находящихся на рабочей поверхности. Данный бокс можно использовать для работы с инфекционными агентами II-III, а также IV групп опасности при наличии подачи воздуха под давлением. Боксы биологической безопасности класса II B1 пригодны для работы с небольшими количествами летучих химикатов и радионуклидов. Для работы со значительными количествами радионуклидов и токсичных химикатов необходим бокс биологической безопасности класса II В2, который также называется боксом с полной сменой отработанного воздуха.
3 ГОСТ Р ЕН 12469-2010:
3.3. Бокс микробиологической безопасности: вентилируемое ограниченное пространство, предназначенное для обеспечения защиты оператора и среды от аэрозолей, возникающих вследствие работы с потенциально опасными и опасными микроорганизмами, с помощью удаления воздуха в атмосферу путем фильтрации.
3.5. БМБ класса II (MSC class II): БМБ с рабочим проемом, через который оператор может проводить манипуляции внутри бокса. Бокс должен быть сконструирован таким образом, чтобы оператор был защищен, риск загрязнения продукта и перекрестного загрязнения низок, а удаление возникающих загрязнений обеспечивалось с помощью профильтрованного воздушного потока, циркулирующего внутри бокса, а также с помощью фильтрации удаляемого из бокса воздуха.
Примечание – Обычным способом обеспечения защиты является создание однонаправленного нисходящего ламинарного воздушного потока внутри бокса и воздушной завесы в рабочем проеме.
4 СанПин РФ 1.3.2322-08 от 28.01.2008 № 4, п. 2.3.30-31: Для обеспечения физической защиты работающего персонала, воздуха и поверхностей рабочей зоны, окружающей среды от исследуемых микроорганизмов должны использоваться боксы биологической безопасности. Для работы с патогенными биологическими агентами должны применяться боксы биологической безопасности II класса.
СанПин РФ 1.3.1325-03, от 22.05.03 № 99 от 30 июня 2003 г., п.3.10: Лабораторию обеспечивают защитными укрытиями II класса для выполнения работ, при которых высока возможность образования аэрозоля (измельчение, гомогенизация, интенсивное встряхивание материалов; вскрытие контейнеров с материалом, давление в которых может оказаться отличным от атмосферного; обращение с материалами высоких концентраций инфекционного агента или больших объёмов).
Приложение № 1 к этому же СП: Бокс биологической безопасности — конструкция, используемая для физической изоляции (удержания и контролируемого удаления из рабочей зоны) вирусов с целью предотвращения возможности заражения персонала и контаминации воздуха рабочей зоны и окружающей среды.
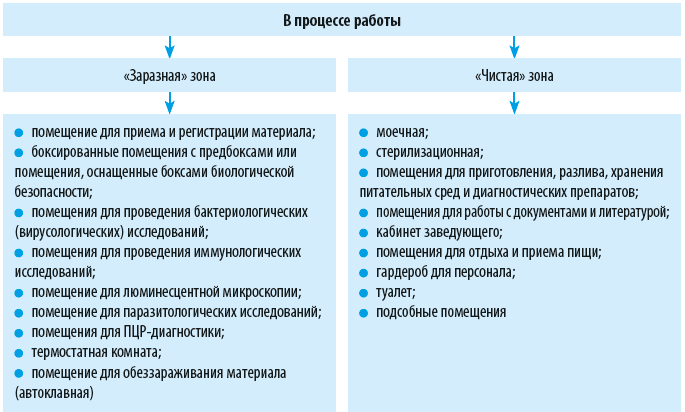
Диагностические лаборатории медицинских организаций, как правило, осуществляют работы с патогенными биологическими агентами (ПБА) III–IV групп патогенности. Чтобы обеспечить в лаборатории требования биологической безопасности, необходимо предусмотреть поточность технологических процессов, зонирование производственных помещений, своевременное проведение дезинфекционных мероприятий. Расскажем о том, как это сделать.
Зонирование лаборатории
Обратите внимание!
Выносить за пределы лаборатории оборудование, лабораторную или хозяйственную посуду, реактивы, инструменты и прочие объекты можно только после их дезинфекции и с разрешения руководителя лаборатории.
Требования к отделке помещений лаборатории
Поверхности пола, стен, потолка, мебели, оборудования и прочих объектов в помещениях лаборатории должны быть гладкими, устойчивыми к влажной уборке с применением моющих и дезинфицирующих средств. Для пола необходимо предусмотреть гидроизоляцию и антискользящее покрытие.
Если лаборатория располагается на первом этаже или в цоколе, то окна обязательно оснащают металлическими решетками, не нарушающими правил пожарной безопасности. Для защиты рабочих столов от попадания прямого солнечного света используют светозащитную пленку или жалюзи из материалов, устойчивых к воздействию дезсредств.
Доставка и прием биологического материала
На дно контейнера для транспортировки укладывают адсорбирующий материал (марлевую салфетку, ткань, вату).
Обратите внимание!
Не допускается доставка материала в хозяйственных сумках, чемоданах, портфелях и других предметах личного пользования.
Чтобы исключить контакт бланков-направлений с биологическим материалом, их вкладывают в отдельный полиэтиленовый пакет.
Важно!
Персонал лаборатории должен осуществлять прием и разбор биологического материала с использованием средств индивидуальной защиты: масок и резиновых перчаток.
Работа с патогенными биологическими агентами
Важно!
Запрещается пипетировать ртом и переливать жидкий инфекционный материал через край пробирки, покидать рабочее место во время манипуляций с ПБА, удалять необеззараженные сгустки крови из пробирок вытряхиванием, сливать жидкие отходы в канализацию без предварительного обеззараживания.
- центрифугирование ПБА и другие манипуляции, вследствие которых образуются аэрозоли;
- приготовление суспензий;
- работа с лиофилизированными ПБА;
- работа по ведению коллекционных штаммов;
- работа по идентификации и изучению выделенных штаммов микроорганизмов.
- серологические исследования и ПЦР-исследованияпо детекции в клиническом материале возбудителей парентеральных вирусных гепатитов В и С, ВИЧ-инфекции и других микроорганизмов II группы патогенности.
Во время работ двери боксов и предбоксов должны быть закрыты. До момента окончания работ выход из боксов не допускается.
Перед началом работ с использованием боксов биологической безопасности включают вентиляцию, проверяют исправность оборудования, наличие аварийного запаса дезинфицирующих средств. Манипуляции с ПБА должны выполняться ближе к задней стенке бокса на поддонах с салфетками, смоченными дезинфицирующим раствором.
После окончания работ с ПБА переднюю панель бокса биологической безопасности опускают, внутри бокса включают бактерицидные лампы.
Обратите внимание!
Боксы биологической безопасности должны проверяться на защитную эффективность:
после монтажа и подготовки к использованию;
после перемещения или ремонта;
не реже одного раза в год при наличии фильтров предварительной очистки воздуха от крупнодисперсных частиц;
не реже 2 раз в год при отсутствии фильтров предварительной очистки воздуха от крупнодисперсных частиц.
При проверке боксов должны контролироваться параметры эффективности работы фильтров очистки воздуха и скорость воздушного потока в рабочем проеме бокса.
Дезинфекционные мероприятия в лаборатории
При организации дезинфекционных мероприятий в лабораториях применяют физические и химические методы дезинфекции.
Для обеззараживания лабораторной посуды, защитной одежды персонала, бактериологических посевов, а также жидких отходов можно применять паровые стерилизаторы.
В воздушных стерилизаторах допускается обеззараживать лабораторную посуду из стекла, металлов или силикона, не загрязненную органическими веществами.
Обратите внимание!
Параметры паровой и воздушной стерилизации контролируют с помощью максимальных термометров, которые размещаются в контрольных точках. Количество контрольных точек зависит от объема камеры стерилизатора. Параметры паровой стерилизации дополнительно контролируются при помощи мановакуумметров.
Химический контроль термической стерилизации осуществляют при каждом цикле работы с использованием специальных тест-индикаторов, необходимое количество и точки расположения которых зависят от вида аппаратуры и объема стерилизационной камеры.
Контроль стерилизации с помощью бактериологических методов (биотестов) должен осуществляться не реже 2 раз в год, а также после ввода в эксплуатацию и ремонта аппаратуры. Биотесты, содержащие некоторое количество жизнеспособных микроорганизмов, обладающих высокой резистентностью, помещают в контрольные точки стерилизационной камеры. При качественно проведенном процессе стерилизации микроорганизмы погибают. Вид применяемых биотестов зависит от типа стерилизационного оборудования.
Химическими методами проводят обеззараживание различных поверхностей, медицинской мебели, оборудования, жидких отходов, спецодежды и других объектов.
К сведению
При выборе химических дезинфектантов предпочтение следует отдавать средствам с широким спектром антимикробной активности.
Объекты, загрязненные кровью, необходимо дезинфицировать растворами, обладающими активностью в отношении возбудителей парентеральных инфекций.
Рабочие растворы дезсредств готовят в специально отведенных помещениях или в вытяжном шкафу. Контейнеры (емкости) с растворами маркируют, указывая название дезсредства и его назначение, концентрацию раствора, дату приготовления и дату конечной реализации.
Дезсредства, применяемые для проведения текущих и генеральных уборок, должны обладать моющими свойствами. Текущую уборку проводят 2 раза в день. Обрабатывают полы, мебель, оборудование, подоконники, двери.
Генеральные уборки проводят не реже 1 раза в месяц, в боксированных помещениях — не реже 1 раза в неделю.
После влажной уборки включают бактерицидные облучатели. Их следует эксплуатировать в соответствии с действующими методическими документами и инструкциями по применению конкретного оборудования.
Обратите внимание!
Если в течение дня нужно экстренно обработать небольшие по площади или труднодоступные поверхности, следует использовать готовые к применению формы дезсредств, которые имеют небольшое время экспозиции и выпускаются в виде спреев или дезинфицирующих салфеток.
Медицинские изделия и посуду дезинфицируют способом полного погружения в рабочий раствор дезинфицирующего средства. Разъемные изделия обеззараживают в разобранном виде, каналы и полости изделий заполняют дезинфицирующим раствором.
Особенности обращения с отходами лабораторий
Лабораторную посуду с культурами микроорганизмов, как правило, обеззараживают в паровых стерилизаторах.
Важно!
Пробирки со сгустками крови обеззараживают с использованием дезинфицирующих растворов или с применением физических методов дезинфекции. Вытряхивать необеззараженные сгустки крови из пробирок запрещено.
При погружении в дезинфицирующий раствор пробирок со сгустками крови необходимо соблюдать осторожность. Пробирку берут анатомическим пинцетом так, чтобы одна его бранша вошла немного внутрь, и погружают ее в наклонном положении до полного заполнения раствором. При правильном погружении воздушные пузыри не образуются, пробирка опускается на дно.
Техника безопасности и ликвидация аварийных ситуаций
Помещения лаборатории должны быть оборудованы пожарной сигнализацией и обеспечены средствами пожаротушения в соответствии с требованиями пожарной безопасности.
Сотрудники диагностических лабораторий должны быть обеспечены спецодеждой соответствующего размера: медицинскими халатами и костюмами, шапочками, медицинской обувью и средствами индивидуальной защиты, в том числе перчатками и масками, респираторами.
Для работы в боксированных помещениях используют отдельный халат, доходящий до нижней трети голени, и тапочки.
Рабочая одежда и обувь должны быть индивидуальными, храниться отдельно от личной одежды. Смена рабочей одежды проводится по мере загрязнения, но не реже 1 раза в неделю. Стирать спецодежду следует централизованно. Перед сдачей в стирку защитную одежду обеззараживают.
Важно!
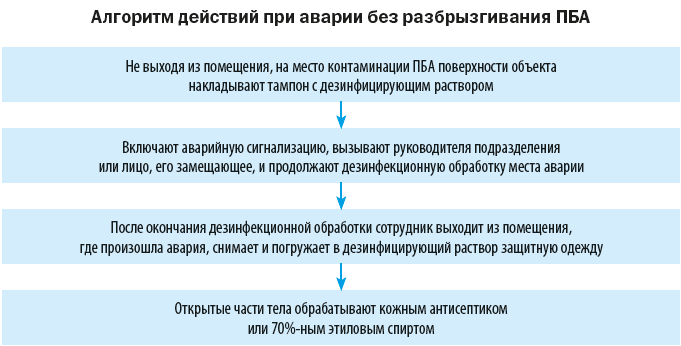
На случай аварийных ситуаций, при которых создается угроза выделения ПБА в воздух рабочей зоны или есть риск заражения персонала, в лаборатории должен быть план ликвидации аварии и запас дезинфицирующих средств.
Объем мероприятий по ликвидации аварии зависит от характера выполняемой работы, вида и свойств ПБА, масштабов аварии.
Кроме того, в специально отведенном месте хранят аварийную аптечку, гидропульт, комплекты рабочей одежды для переодевания пострадавших и защитной одежды для сотрудников, ликвидирующих последствия аварии. Ответственным за комплектование аптечки и аварийной укладки является заведующий лабораторией.
Состав аварийной аптечки:
1. Спирт этиловый 70%-ный — 2 флакона по 100 мл.
2. Спиртовой раствор йода 5%-ный — 1 флакон.
3. Раствор борной кислоты 1%-ный — 1 флакон.
4. Нашатырный спирт — 1 флакон.
5. Бинт марлевый медицинский стерильный (5 м × 10 см) — 2 шт.
6. Лейкопластырь бактерицидный (не менее 1,9 см × 7,2 см) — 3 шт.
7. Салфетка марлевая медицинская стерильная (не менее 16 см × 14 см, № 10) — 1 уп.
8. Ножницы с закругленными браншами.
При аварии во время работы на центрифуге крышку медленно открывают только спустя 30–40 минут, чтобы сформировавшийся аэрозоль успел осесть. Центрифужные стаканы и разбитое стекло помещают в дезинфицирующий раствор, поверхность крышки, внутренние части центрифуги, ее наружную поверхность дезинфицируют (после отключения ее от электросети).
О каждом случае аварийной ситуации руководитель лаборатории обязан сообщить комиссии по контролю соблюдения требований биологической безопасности, а также руководителю медорганизации.
Не реже 1 раза в год в лаборатории должны проводиться тренировочные учения по ликвидации аварий.
Допуск персонала к работе с ПБА
Допуск персонала к работе с ПБА III–IV групп патогенности, а также допуск инженерно-технического персонала к обслуживанию лабораторного оборудования должен осуществляться на основании приказа главного врача. Приказ издается не реже одного раза в два года, корректируется по мере необходимости.
В лабораториях медорганизаций работу с ПБА могут выполнять специалисты не моложе 18 лет с высшим и средним медицинским или биологическим образованием, прошедшие необходимую профессиональную подготовку.
Лица, имеющие медицинские противопоказания к вакцинации, лечению специфическими препаратами, использованию средств индивидуальной защиты, к работам с ПБА не допускаются.
Не реже 1 раза в год медицинский персонал, работающий с ПБА, должен проходить инструктаж по соблюдению требований биологической безопасности. Инженерно-технический персонал, дезинфекторы и санитарки лаборатории также должны проходить вводные и периодические инструктажи по биологической безопасности.
При приеме на работу сотрудников лаборатории направляют на предварительный медицинский осмотр для выявления противопоказаний с учетом специфики трудовой деятельности[1].
Все сотрудники, которые привлекаются к работам с ПБА, должны быть привиты в соответствии с календарем профилактических прививок и календарем прививок по эпидемическим показаниям.
К работе с паровыми стерилизаторами (автоклавами) могут быть допущены лица, обученные, аттестованные и имеющие удостоверение на право обслуживания сосудов, работающих под давлением.
Организация работы комиссии по биологической безопасности
Для контроля за соблюдением мер биологической безопасности при работе с ПБА в медорганизации создается специальная комиссия. В ее состав, как правило, включают заведующего лабораторией, врача-эпидемиолога или его помощника, инженера по охране труда и других заинтересованных специалистов.
Задачи комиссии по биологической безопасности:
- организация и проведение постоянного контроля за соблюдением регламентированного порядка обеспечения биологической безопасности лаборатории;
- разработка комплекса мер по совершенствованию биологической безопасности;
- организация и проведение мероприятий, направленных на предупреждение аварийных ситуаций при работе с ПБА и ликвидацию их последствий;
- контроль за подготовленностью сотрудников к работе с ПБА и организация наблюдения за состоянием их здоровья.
Заседания комиссии проводятся не реже 2 раз в год. Решения комиссии доводятся до сведения руководителя медорганизации.


ОСОБЕННОСТИ РАБОТЫ В МИКРОБИОЛОГИЧЕСКОЙ ЛАБОРАТОРИИ. ТЕХНИКА И МЕТОДИКА ПОСЕВОВ. МЕТОДЫ ОСНОВНЫХ МИКРОБИОЛОГИЧЕСКИХ ОПРЕДЕЛЕНИЙ. АСЕПТИКА И АНТИСЕПТИКА УЧЕБНЫЙ МОДУЛЬ № 2

ОСОБЕННОСТИ РАБОТЫ В МИКРОБИОЛОГИЧЕСКОЙ ЛАБОРАТОРИИ • Микробиологическая лаборатория включает ряд помещений, где проводят работу с микроорганизмами или подготовку к ней. • Под лабораторные комнаты отводят наиболее светлые, просторные помещения, естественная освещенность которых должно составлять не менее 110 лк. Поверхность столов и пол всех лабораторных помещений покрывают легко моющимся материалом — пластиком или линолеумом, а стены на высоту 170 см от пола окрашивают в светлые тона. Основное рабочее помещение оборудовано столами лабораторного типа, шкафами и полками для хранения аппаратуры, посуды и реактивов. Столы имеют подводку электроэнергии и снабжены

ЛАБОРАТОРИЯ • Кроме основного рабочего помещения лаборатория имеет стерилизационную , где размещены автоклавы и сушильные шкафы, термостатированную комнату для выращивания микроорганизмов, помещение для хранения культур микроорганизмов, холодильную комнату, моечную. • Пересевы микроорганизмов осуществляют в боксах разных конструкций - от изолированных помещений до настольных камер (ламинаров), чистота атмосферы рабочего пространства в

РАБОТА В ЛАМИНАРНОМ БОКСЕ • Ламинарные боксы бывают двух степеней защиты — класса I и класса II. • Ламинары класса I оборудованы притяжной вентиляцией нестерильного воздуха из помещения и выходом этого воздуха в то же помещение после фильтрации (защита от микробных аэрозолей) и в строгом смысле слова не пригодны для стерильной работы. • Ламинары с защитой класса II образуют внутри бокса поток стерильного воздуха, забор которого происходит из помещения, и который стерилизуется, проходя через бактериальные фильтры. Таким образом, внутренние поверхности бокса остаются стерильными. Конструкция позволяет также проводить стерильные посевы микроорганизмов в струе стерильного воздуха, прошедшего через бактериальные фильтры и распределенного внутри

ПОДГОТОВКА БОКСА ЛАМИНАРНОГО БОКСА К РАБОТЕ • Перед началом работы ламинар должен быть вымыт с помощью растворов нейтральных детергентов и все доступные внутренние его поверхности должны быть простерилизованы химическими дезинфектантами (70%- й этанол). В течение работы ламинар необходимо мыть раз в месяц, снимая съемные детали поверхности и прочищая пространство под ними. После промывки панели прибора вновь стерилизуют этанолом. • Бактериальные фильтры ламинара необходимо подвергать процессу химической дезинфекции один раз в течение 1 - 2 мес. в зависимости от интенсивности использования. Химическую дезинфекцию внутренней поверхности ламинара и в особенности его фильтров проводят парами формальдегида. С этой целью 50 мл 37%-го раствора формальдегида (формалин) наливают в фарфоровую чашку, ставят на подставку и нагревают чашку для медленного (30 мин) испарения

ОБРАБОТКА ПОМЕЩЕНИЙ МИКРОБИОЛОГИЧЕСКОЙ ЛАБОРАТОРИИ • Пол , стены и мебель в микробиологической лаборатории обрабатывают пылесосом и протирают раствором различных дезинфицирующих веществ. Обработка пылесосом обеспечивает освобождение предметов от пыли и удаление с них значительного количества микроорганизмов. Установлено, что при 4 - кратном проведении щеткой пылесоса по поверхности предмета с него удаляется примерно 47% микроорганизмов, а при 12 -кратном - до 97%. • В качестве дезинфицирующих растворов чаще всего пользуются 2 - 3%-м раствором соды (бикарбоната натрия), 3 - 5%-м водным раствором фенола (карболовой кислоты) или лизола (препарата фенола с добавлением зеленого мыла), 0, 5 -3%-м водным раствором хлорамина и некоторыми другими дезинфектантами.

ВОЗДУХ В ЛАБОРАТОРИИ ОЧИЩАЮТ ПРОВЕТРИВАНИЕМ - ЭТО НАИБОЛЕЕ ПРОСТОЙ СПОСОБ • Но наиболее эффективный и часто применяемый способ дезинфекции воздуха - ультрафиолетовое облучение лучами с длиной волны от 260 нм. Эти лучи обладают высокой антимикробной активностью и могут вызывать гибель не только вегетативных клеток, но и спор микроорганизмов. • Воздействие ультрафиолетовых лучей должно быть непосредственным и длительным. Это связано, прежде всего с тем, что ультрафиолетовые лучи обладают слабой проникающей способностью. Например, они не проходят через обычное стекло, легко поглощаются частицами пыли. Кроме того, листы белой бумаги, пластины алюминия и хрома, а также предметы, изготовленные из них, могут заметно отражать ультрафиолетовые лучи. Поэтому в зависимости от степени загрязнения воздуха для его стерилизации требуется облучение от 30 мин до

В КАЧЕСТВЕ ИСТОЧНИКА УЛЬТРАФИОЛЕТОВОГО ИЗЛУЧЕНИЯ ИСПОЛЬЗУЮТСЯ БАКТЕРИЦИДНЫЕ ЛАМПЫ • Излучателем в них служит электрическая дуга, возникающая в парах ртути низкого давления. Более 80% испускаемого ими спектра приходится на волну длиной 254 нм. Обычно бактерицидные лампы представляют собой трубки различного диаметра и длины, изготовленные из специального стекла, пропускающего излучение с длиной волны 254 нм. Каждая трубка вмонтирована в корпус-держатель и может быть снабжена отражателем. Необходимо иметь в виду, что ультрафиолетовые лучи могут вызывать тяжелые поражения глаз, поэтому при работе с бактерицидными лампами нужно строго следить за тем, чтобы ни прямые, ни отраженные ультрафиолетовые лучи не попадали в глаза. В небольших помещениях при включенной бактерицидной лампе находиться нельзя. Следует также учитывать, что при длительной непрерывной работе бактерицидной лампы интенсивность излучения

РАБОЧЕЕ МЕСТО, ГДЕ НЕПОСРЕДСТВЕННО РАБОТАЮТ С КУЛЬТУРАМИ МИКРООРГАНИЗМОВ, ТРЕБУЕТ ОСОБЕННО ТЩАТЕЛЬНОЙ ОБРАБОТКИ • Рабочий стол следует дезинфицировать не только до начала работы, но и после ее окончания. • Для протирания поверхности стола можно использовать растворы лизола и хлорамина, а также 70%-е (по объему) растворы изопропилового или этилового спиртов. Спирты весьма эффективны в отношении вегетативных форм микроорганизмов. Названные спирты можно также применять для дезинфекции рук. В тех случаях, когда поверхность стола имеет водоотталкивающее покрытие, особенно удобен лизол. Поверхность рабочего стола можно дезинфицировать и ультрафиолетовыми лучами. При этом следует учитывать, что бактерицидное действие лучей тем выше, чем ближе облучаемая поверхность к

ЗАПРЕЩАЕТСЯ ! • В лаборатории не разрешается курить, хранить и употреблять еду, напитки, жевательную резинку. • Работать следует в халатах и при необходимости в комплектах защитнойодежды.

ТЕХНИКА И МЕТОДИКА ПОСЕВОВ • Техника посева микроорганизмов в жидкие, полужидкие и на плотные питательные среды • Посев уколом • Посев на плотную среду в чашки Петри

ТЕХНИКА БЕЗОПАСНОСТИ • При выполнении исследований по изучению: • способов приготовления питательных сред; • подготовки посуды для культивирования микроорганизмов; • изучению состава питательных сред и техники посевов культур микробов в жидкие, полужидкие и на плотные среды • необходимо неукоснительно соблюдать правила, обязательные при работе с культурами микроорганизмов, газовыми горелками, сосудами, работающими под давлением (автоклавы), лабораторной стеклянной посудой, электрооборудованием.

МЕТОДЫ ОСНОВНЫХ МИКРОБИОЛОГИЧЕСКИХ ОПРЕДЕЛЕНИЙ • МЕТОДЫ КОЛИЧЕСТВЕННОГО УЧЕТА МИКРООРГАНИЗМОВ: • ОПРЕДЕЛЕНИЕ КОЛИЧЕСТВА КЛЕТОК С ПОМОЩЬЮ СТАНДАРТА МУТНОСТИ; • СЧЕТНОЙ КАМЕРЫ; • ЧАШЕЧНЫЙ МЕТОД КОХА.

ОБЩИЕ ПОНЯТИЯ • О росте микроорганизмов в естественных субстратах или в питательных средах микробиологи судят по изменению количества клеток или биомассы микробов в процессе их культивирования. Такой подход основан на способности микроорганизмов размножаться, т. е. начинать и завершать клеточное деление, что предполагает возможность контроля увеличивающегося числа бактериальных дискретных единиц. При этом используются разные методы контроля (определения) количества клеток микроорганизмов: визуальным сравнением со стандартом мутности; нефелометрическим анализом культур; микроскопическим подсчетом микробных частиц в определенном объеме с применением счетных камер; электронно-микроскопическим подсчетом бактерий, проходящих через соответствующий канал (жиклер); путем

АСЕПТИКА И АНТИСЕПТИКА • 1) Комплекс мер по подавлению роста и размножения потенциально опасных для здоровья человека микроорганизмов при проведении полостных операций. Включает стерилизацию операционного белья, хирургического инструмента, воздуха в операционных. Впервые применена английским хирургом Дж. Листером в 1867 г. • 2 ) Метод консервации материалов и изделий путем обработки их биоцидами- пропитка деревянных железнодорожных шпал креозотом. • В практической микробиологии термин асептика используется для аналогичных мер, предпринимаемых при выращивании чистых культур микроорганизмов с целью предупреждения их контаминации (стерилизация
Читайте также: